Cho 9,15 g hỗn hợp g gồm Cu Al Zn vào dung dịch HCl dư thu được 4,48 l khí H2 điều kiện tiêu chuẩn và 3,2 g một chất rắn x không tan vào dung dịch Y Sau đó lọc Bỏ chất rắn X cô cạn dung dịch Y thu được một lượng muối khan Z a/ Viết phương trình phản ứng hóa học xảy ra b/ Tính khối lượng muối Z
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Đặt số mol FeO, Fe3O4 và Cu lần lượt là x, y, z mol
→ 72x + 232 y + 64z =32,32
Muối gồm FeCl2:x+y (mol);
CuCl2: z mol
→ cô cạn X thu được
mmuối = 127 (x + y) + 135.z = 56,52
Ta có :
3Fe+8/3+2e→3Fe+2
Cu → Cu+2 + 2e

→ 2y = 2z
Do đó x = 0,12 mol và y = z = 0,08 mol
dd thu được có NaNO3 và NaOH do
Dd Y có nNO3 < 1,5 mol
→ nNaNO3 < 1,5 mol
→ NaOH còn dư
→ 104,6 g rắn có x mol NaNO2 và y mol NaOH
→ 69x + 40y =104,6
Bảo toàn Na có x + y = 1,6 mol
→ x =1,4 mol và y =0,2 mol
Bảo toàn nguyên tố N ta có
nHNO3 = nNO3(Y) + nN(khí)
→ 1,5 = 1,4 + nN(khí)
→ nN(khí) =0,1 mol
Đặt số mol O trong khí là a thì
Bảo toàn electron ta có
x + y + 2z + 2a= 5nN trong khí
→ a = 0,07 mol
Khối lượng dung dịch Y là
mdd Y = mrắn + mdd HNO3 – mN (khí) – mO(khí)
= 32,32 + 240 -0,1.14-0,07.16 = 269,8 g
nFe(NO3)3 = 0,12 + 0,08.3 = 0,36 mol
→ C%[Fe(NO3)3] = 32,29%

Đáp án B
nH2 = 0,35 => nCl- = nHCl = 2nH2 = 0,7
=> mMg + mAl = 9,14 – 2,54 = 6,6g => mmuối = 6,6 + 0,7.35,5 = 31,45g

Đáp án B
Sơ đồ tổng quát: (Cu,Mg,Al) + HCl → (MgCl2,AlCl3) + H2 + Cu
nH2 = 7,84: 22,4 = 0,35 mol ; Chất rắn Y chính là Cu không phản ứng với HCl
Bảo toàn nguyên tố: nHCl = 2nH2 = 2.0,35 = 0,7 mol = nCl
mmuối Z = mMg,Al + mCl = (mhh đầu - mCu) + mCl = (9,14 – 2,54) + 35,5.0,7 = 31,45g


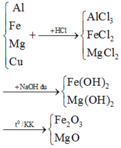


a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có :
\(n_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_{HCl}=2n_{H2}=0,2.2=0,4\left(mol\right)\)
BTKL,
\(m_{hh}+m_{HCl}=m+m_{H2}+m_{Cu}\)
\(\Rightarrow m=9,15+0,4.36,5-0,2.2-3,2=20,15\left(g\right)\)