hỗn hợp gồm NaCl, NaBr , trong đó NaBr chiếm 10% về khối lượng. Hòa tan hỗn hợp vào nước rồi cho khí clo lội qua dd cho đến dư. Làm bay hơi dd cho đến khi thu được muối khan. Khối lượng hỗn hợp đầu đã thay đổi bao nhiêu% ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi a, b lần lượt là số mol của NaI và NaBr ban đầu, ta có : Sơ đồ phản ứng:
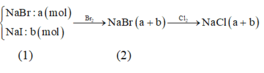

Đáp án A

\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\left(1\right)\\ m_{giảm}=m_{Br_2}-m_{Cl_2}\\ \Leftrightarrow n_{NaCl\left(1\right)}=n_{NaBr\left(1\right)}=\dfrac{13,35}{160-71}=0,15\left(mol\right)\\ \Rightarrow\%m_{NaBr}=\dfrac{103.0,15}{42,6}.100\approx36,268\%\\ \Rightarrow\%m_{NaCl}\approx63,732\%\)
Bổ sung:
\(C\%_{ddNaBr\left(trongA\right)}=\dfrac{0,15.103}{200}.100=7,725\%\\ C\%_{ddNaCl\left(trongA\right)}=\dfrac{42,6-0,15.103}{200}.100=13,575\%\)

NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%

Gọi số mol NaCl, NaI là a, b (mol)
=> 58,5a + 150b = 37,125 (1)
PTHH: 2NaI + Cl2 --> 2NaCl + I2
b------------>b
=> nNaCl(sau pư) = a + b = \(\dfrac{23,4}{58,5}=0,4\left(mol\right)\) (2)
(1)(2) => a = 0,25 (mol); b = 0,15 (mol)
=> \(\left\{{}\begin{matrix}\%m_{NaCl}=\dfrac{58,5.0,25}{37,125}.100\%=38,4\%\\\%m_{NaI}=\dfrac{0,15.150}{37,125}.100\%=60,6\%\end{matrix}\right.\)
=> A
Gọi \(\left\{{}\begin{matrix}n_{NaCl}=x\left(mol\right)\\n_{NaI}=y\left(mol\right)\end{matrix}\right.\)\(\Rightarrow58,5x+150y=37,125\left(1\right)\)
\(n_{NaCl}=\dfrac{23,4}{58,5}=0,4mol\)
\(\Rightarrow x+y=0,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,25mol\\y=0,15mol\end{matrix}\right.\)
\(\%m_{NaCl}=\dfrac{0,25\cdot58,5}{37,125}\cdot100\%=39,4\%\)
\(\%m_{NaI}=100\%-39,4\%=60,6\%\)
Chọn A

Coi mhh=100g
⇒mNaBr=10.mNaCL=90(g)
Cl2+2NaBr→2NaCl+Br2
\(\frac{10}{103}\rightarrow\frac{10}{103}\rightarrow\frac{5}{103}\)
⇒mNaCl tạo thành =\(\frac{10}{103}\).58,5=5,68(g)
Có: mBr2 sau phản ứng = 7,767
⇒ m sau phản ứng =90+5,68+7,767=103,45(g)
Vậy sau phản ứng m tăng lên 3,45g và tăng 3,45% so với ban đầu

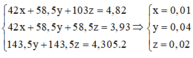
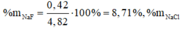
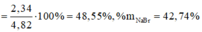
Ta xét mhh = 100gam => mNaBr = 10g; mNaCl = 90g
=> mNaBr = 10/103 mol
2NaBr + Cl2 -> 2NaCl + Br2
\(\frac{10}{103}\)--------------->\(\frac{10}{103}\)
=> mNaCl = \(\frac{10}{103}\)*58,5 = 5,68 gam
=> Tổng khối lượng muối NaCl sau pứ = 90 + 5,68 = 95,68 gam < 100gam
=> Khối lượng muối sau pứ giảm (100-95,68)= 4,32 gam ~ \(\frac{4,32}{100}\cdot100\%=4,32\%\)
Coi \(m_{hh}=100\left(g\right)\)
\(\Rightarrow m_{NaBr}=10.n_{NaCl}=90\left(g\right)\)
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
10/103___10/103_______5/103
\(\Rightarrow n_{NaCl}\) tạo thành = \(\frac{10}{103}.58,5=5,68\left(g\right)\)
Có: mBr2 sau phản ứng = 7,767
\(\Rightarrow m_{sau.phan.ung}=90+5,68+7,767=103,45\left(g\right)\)
Vậy sau phản ứng m tăng lên 3,45g và tăng 3,45% so với ban đầu.