NTK trung bình của nguyên tố R là 79,91. Biết R có 2 đồng vị, trong đó 1 đồng vị là 79R chiếm 54.5% số nguyên tử. Số khối của đồng vị thứ 2 là:
A.81 B.85 C.82 D.80
Mọi người ơi ! Mình còn 39 câu nữa :((( Giúp mình giải hết được hong :((((
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
- Phần trăm của đồng vị còn lại là 100% - 54,5% = 45,5%
- Công thức tính nguyên tử khối trung bình:
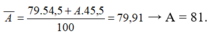

Đặt x nguyên tử khối của đồng vị còn lại
Ta có : \(\overline{M}=\dfrac{54,5.79+\left(100-54,5\right).x}{100}=79,91\)
\(\rightarrow x=81\)
Vậy nguyên tử khối của đồng vị còn lại : \(^{81}X\)

a), Đặt đồng vị thứ 2 của đồng là A2.
\(\overline{NTK}_{Cu}=63,54\\ \Leftrightarrow\dfrac{63.73\%+A_2.27\%}{100\%}=63,54\\ \Leftrightarrow A_2=65\left(đ.v.C\right)\)
b, Khi có 81 nguyên tử đồng vị thứ 2 thì số nguyên tử 63Cu là:
\(\dfrac{81.73}{27}=219\left(nguyên.tử\right)\)
c) Phần trăm khối lượng đồng vị 63Cu có trong phân tử Cu2O là:
\(73\%.\dfrac{63,54.2}{63,54.2+16}\approx64,837\%\)

- Đồng vị thứ nhất có:A1=35+44=79
- Đồng vị thứ 2 có: A2=79+2=81
\(\overline{A}=\dfrac{27.79+23.81}{27+23}=79,92\)

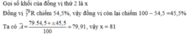

Bn vui lòng đăng lại câu hỏi này ở box Hóa để đc các bn thực sự có năng khiếu với Hóa hơn giúp nhé.
Xin lỗi mình đăng nhầm :((((