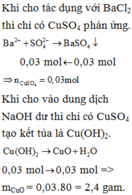
: Hỗn hợp X gồm FeO, Al2O3, MgO. Lâý 61,2 gam hỗn hợp X chia làm 2 phần bằng nhau : Phần 1 : hoà tan vào 200ml dung dịch KOH 1M vừa đủ thu được chất rắn A. Phần 2 : hoà tan vào 500g dung dịch H2SO4 10,78% thu được dung dịch B có khối lượng là 529,6 gam.Cho V lít Ba(OH)2 0,5 M vào dd B thu được chất rắn C. Để C ngoài không khí thu được chất rắn D a. Tính % khối lượng mỗi oxit có trong hỗn hợp X. b. Tính C% ddB. c. Tính V để d có giá trị lớn nhất, nhỏ nhất
mn giúp e với ạ
e cảm ơn ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Gọi số mol của Na2O và Al2O3 trong từng phần là x và y
Phần 1:
Ta có các phương trình phản ứng:
Na2O + H2O → 2NaOH
x → 2x
2NaOH + Al2O3 → 2NaAlO2 + H2O
2x → x
Chất rắn không tan là Al2O3
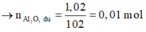
=> y = x + 0,01 (1)
Phần 2:
nHCl = 0,14.1 = 0,14 mol
Ta có phương trình phản ứng:
Na2O + 2HCl → 2NaCl + H2O
Al2O3 + 6HCl → 2AlCl3 + 3H2O
nHCl = 2x + 6y = 0,14 (2)
Từ (1) và (2) ta có: x = 0,01, y = 0,02
![]()
= 2.(0,01.62 + 0,02.102) = 5,32

Đáp án C.
Gọi số mol của Na2O và Al2O3 trong một phần là x và y mol.
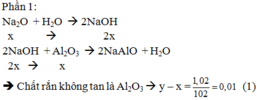
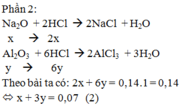
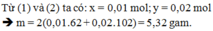

Đáp án : C
P1 : nBaCO3 = nR2CO3 + nRHCO3 = 0,11 mol
=> Mtrung bình = 85,18g
=> 12,59 < R < 24,18
=> R là Na hoặc NH4
P2 : Nhiệt phân : 2RHCO3 -> R2CO3 + CO2 + H2O
=> mgiảm = mCO2 + mH2O > 3,41g
=> nRHCO3 > 0,11 mol Vô lý
=> R là NH4 => n(NH4)2CO3 = 0,04 ; nNH4HCO3 = 0,07 mol
=> VKOH = 0,04.2 + 0,07.2 = 0,22 lit = 220 ml

\(n_{H_2}=\dfrac{4,928}{22,4}=0,22mol\)
\(n_{CuSO_4}=0,66.0,5=0,33mol\)
- Gọi số mol trong phần I là :Fe(x mol), Al(y mol), Ag(z Mol)
- Sỗ mol mỗi kim loại trong phần II: Fe(tx mol), Al(ty mol), Ag(tz Mol)
56(x+tx)+27(y+ty)+108(z+tz)=24,5(*)
- Phần I: Fe+2HCl\(\rightarrow\)FeCl2+H2(1)
2Al+6HCl\(\rightarrow\)2AlCl3+3H2(2)
x+1,5y=0,22(**)
- Phần II: Fe+CuSO4\(\rightarrow\)FeSO4+Cu(3)
2Al+3CuSO4\(\rightarrow\)Al2(SO4)3+3Cu(4)
tx+1,5ty=0,33(***)
152tx+171ty=39,9(****)
- Kết hợp(***) và(****) : tx=0,06, ty=0,18
\(y=3x\)(*****)
- kết hợp (**) và (*****) ta có: x=0,04, y=0,12
\(\rightarrow t=\dfrac{0,06}{0,04}=1,5\)
- Thay x=0,04 ,y=0,12 , t=1,5 vào (*) ta có z=0,04
mI=56x+27y+108z=56.0,04+27.0,12+108.0,04=9,8 gam
số mol Cu=tx+1,5ty=0,33 mol
chất rắn Z gồm 0,33 mol Cu và tz=0,04.1,5=0,06 mol Ag
mZ=0,33.64+0,06.108=27,6 gam

Để giải quyết câu hỏi này, chúng ta cần biết rằng glucozơ và saccarozơ đều có công thức phân tử là C12H22O11. Khi tác dụng với dung dịch AgNO3/NH3, mỗi nhóm -CHO trong glucozơ và -CH2OH trong saccarozơ sẽ tạo ra 1 phân tử Ag. Do đó, mỗi phân tử glucozơ sẽ tạo ra 5 phân tử Ag, còn mỗi phân tử saccarozơ sẽ tạo ra 8 phân tử Ag.
Từ đó, ta có thể viết được hệ phương trình sau:
```
`5x + 8y = 16.2/108`
`10x + 8y = 37.8/108`
```
Giải hệ phương trình trên, ta được x = 0.3 mol và y = 0.1 mol.
Vậy khối lượng glucozơ và saccarozơ trong hỗn hợp đầu lần lượt là: `0.3 * 180 = 54 (g)` và 0.1 * 342 = 34.2 (g).
Do đó, đáp án chính xác là A. 27g và 34,2 g.