Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8 lít O2.Xác định CTPT của A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


n C O 2 = 13,2 44 = 0,3 m o l → n C = 0,3 m o l ; m C = 3,6 g a m . n H 2 O = 5,4 18 = 0,3 m o l → n H = 0,6 m o l ; m H = 0,6 g a m .


Vậy A có công thức đơn giản nhất là C H 2 O n .
Lại có M A = 15 . 4 = 60 ( g / m o l ) → n = 2 thỏa mãn.
A là C 2 H 4 O 2 .
⇒ Chọn B.

\(n_{O_2}=0,7\left(mol\right)\)
Gọi: nCO2 = nH2O = a (mol)
Ta có: mX + mO2 = mCO2 + mH2O
⇒ 9,4 + 0,7.32 = 44a +18a ⇒ a =
Đến đây thì ra số mol hơi xấu, bạn xem lại đề nhé.

Đáp án C
1 mol X + 2 mol H2O → 2 mol Y + 1 mol Z chứng tỏ X là tripepit chứa 2 Y và 1 Z.
Đốt cháy Z : nO2 = 0,375 mol, nCO2 = 0,3 mol, nH2O = 0,35 mol, nN2 = PV RT = 1 . 1 , 23 0 , 082 . 300 = 0,05 mol
Bảo toàn khối lượng → m2 = 13,2 + 6,3 + 0,05. 28 - 0,375. 32 = 8,9 gam → loại C
Luôn có nC (Z) = nCO2 = 0,3 mol, nH (Z) = 2nH2O = 0,7 mol, nN(Z) = 2nN2 = 0, 1 mol
→ nO (Z) = 8 , 9 - 0 , 3 . 12 - 0 , 7 - 0 , 1 . 14 16 = 0,2 mol
→ C : H : N : O = 0,3 : 0,7 : 0,1 : 0,2 = 3: 7 : 1:2 → công thức của Z là C3H7NO2
Vậy nY= nH2O = 2nZ = 0,2 mol
Bảo toàn khối lượng cho phản ứng thủy phân → m1 = 20,3 + 0,2. 18 - 8,9 = 15 gam
→ MY = 15 : 0,2 = 75 → Y có cấu tạo H2N-CH2-COOH.
Vậy Y : H2N-CH2-COOH (15 gam) và Z : CH3-CH(NH2)-COOH ( 8,9 gam).

a)
Do \(\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1}{2}\)
=> \(\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
Giả sử A có CTHH là CxH4xOy
Gọi số mol của A là a (mol)
=> 12ax + 4ax + 16ay = 3,2
=> ax + ay = 0,2 (1)
Bảo toàn C: nCO2 = ax (mol)
Bảo toàn H: nH2O = 2ax (mol)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn O: \(ay+0,4.2=2ax+2ax\)
=> 4ax - ay = 0,8 (2)
(1)(2) => ax = 0,2 (mol); ay = 0 (mol)
=> A chỉ chứa C và H
\(\left\{{}\begin{matrix}n_C=ax\left(mol\right)\\n_H=4ax\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_C=12.ax=2,4\left(g\right)\\m_H=1.4ax=0,8\left(g\right)\end{matrix}\right.\)
b)
Xét \(\dfrac{n_C}{n_H}=\dfrac{1}{4}\)
=> CTPT: (CH4)n
Mà M = 16 g/mol
=> n = 1
=> CTPT: CH4

nC = nCO2 = 8,8/44 = 0,2 (mol)
nH = 2 . nH2O = 2 . 5,4/18 = 0,6 (mol)
nO = (4,6 - 0,2 . 12 - 0,6)/16 = 0,1 (mol)
CTPT: CxHyOz
=> x : y : z = 0,2 : 0,6 : 0,1 = 2 : 6 :1
(C2H6O)n = 46
=> n = 1
=> CTPT: C2H6O

\(TrongA:n_C=n_{CO_2}=0,15\left(mol\right)\\ n_H=2n_{H_2O}=0,3\left(mol\right)\\ \Rightarrow n_O=\dfrac{4,5-12.0,15-0,3.1}{16}=0,15\left(mol\right)\\ \Rightarrow CTPT:C_xH_yO_z\\ Tacó:x:y:z=0,15:0,3:0,15=1:2:1\\ \Rightarrow CTĐGN:\left(CH_2O\right)_n\\ Tacó:\left(12+2+16\right).n=60\\ \Rightarrow n=2\\ Vậy:CTHHcủaA:C_2H_4O_2\)

n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
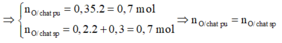
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
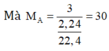
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.

Đáp án : B
Đặt nCO2 = nH2O = x; bảo toàn khối lượng => X = 0,3 mol
Bảo toàn C và H => nO = 0,1; Tỉ lệ C:H:O = 3 : 6 : 1
\(n_{CO2}=0,3\left(mol\right),n_{H2O}=0,35\left(mol\right)\)
Theo bảo toàn khối lượng
m A+mO2=mCO2+mH2O
\(\rightarrow4,3+m_{O2}=0,3.44+0,35.18\)
\(\rightarrow m_{O2}=15,2\rightarrow n_{O2}=0,475\left(mol\right)\)
BT Oxi: nO trong A+2nO2=2nCO2+nH2O
\(\rightarrow\) nO trong A=0
\(\rightarrow\)Trong A không có O
Gọi công thức A là (CxHy)n
Ta có \(x:y=n_C:n_H=0,3:0,7=\frac{3}{7}\)
Vậy A là (C3H7)n
Ta có
\(C_{3n}H_{7n}+4,75n_{O2}\rightarrow3n_{CO2}+3,5n_{H2O}\)
0,1______0,475n__________________
Ta có \(n_{O2}=0,475=\frac{212,8}{22,4}=9,5\)
\(\rightarrow n=20\)
Vậy Công thức là C60H140