hòa tan hoàn toàn 10,1g hỗn hợp 2 kl kiềm ở 2 chu kì liên tiếp vaof nước, thu được 3,36l H2 (đktc) . phần trăm theo kl của mỗi kl trong hỗn hợp là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


ĐÁP ÁN A
X + H2O -> XOH + ½ H2
=> nKL = 2nH2 = 0,3 mol
=> Mtb = 28,33 => X là Na : x mol và Y là K : y mol
=> 23x + 39y = 8,5 và x + y = 0,3
=> x = 0,2 ; y = 0,1 mol
=> %mNa(hh) = 54,12%

a)
Gọi CTTQ của hai kim loại nhóm IA là R
\(n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ 2R + 2H_2O \to 2ROH + H_2\)
Theo PTHH :
\(n_R = 2n_{H_2} = 0,4(mol)\\ \Rightarrow R = \dfrac{11,6}{0,4} = 29(g/mol)\)
Ta thấy : \(M_{Na} = 23 < 29 < M_{K} = 39\)
Vậy hai kim loại cần tìm là Natri,Kali
b)
Gọi \(n_{Na} = a(mol) ; n_K = b(mol)\)
Ta có :
\(23a + 39n = 11,6\\ a + b = 0,4\)
Suy ra : a = 0,25 ; b = 0,15
Vậy :
\(\%m_{Na} = \dfrac{0,25.23}{11,6}.100\% = 49,57\%\\ \%m_{K} = 100\% - 49,57\% = 50,43\%\)
c)
Sau phản ứng,mdung dịch = 11,6 + 108,8 - 0,2.2 = 120(gam)
\(n_{NaOH} = n_{Na} = 0,25\ mol\\ n_{KOH} = n_K = 0,15\ mol\)
Suy ra :
\(C\%_{NaOH} = \dfrac{0,25.40}{120}.100\% = 8,33\%\\ C\%_{KOH} = \dfrac{0,15.56}{120}.100\% = 7\%\)

Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 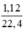 = 0,05(mol)
= 0,05(mol)
PTHH: 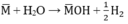
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 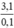 = 31 → Na, K
= 31 → Na, K
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
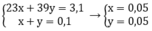
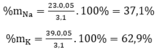

Giải thích:
nH2 = 3,36/ 22,4 = 0,15 (mol)
Gọi công thức chung của 2 kim loại kiềm là M
2M + 2H2O → 2MOH + H2↑
0,3 ← 0,15 (mol)
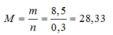
=> Mx < 28,33 < MY và X, Y là 2 kim loại kiềm kế tiếp => X là kim loại Na, Y là kim loại K
Na: x ( mol) ; K: y (mol)
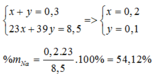
Đáp án B

\(n_{H2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
Đặt CTTB của hai kim loại kiềm là \(\overline{R}\)
PTHH : \(2\overline{R}+2H_2O-->2\overline{R}OH+H_2\uparrow\)
Theo pthh : \(n_{\overline{R}}=2n_{H2}=0,8\left(mol\right)\)
=> \(M_{\overline{R}}=\frac{20,02}{0,8}=25,025\) (g/mol)
Mà hai kim loại kiềm ở hai chu kì liên tiếp => \(\hept{\begin{cases}Natri:23\left(Na\right)\\Kali:39\left(K\right)\end{cases}}\)

- Vì hỗn hợp 2 kim loại kiềm ở 2 chu kì kế nhau lên hỗn hợp kim loại kim loại đó sẽ gồm 2 kim loại : Na, K .
PTHH ( I ) : \(2Na+2H_2O\rightarrow2NaOH+H_2\)
........................x...........x...................x..........\(\frac{1}{2}\)x...........
PTHH ( II ) : \(2K+2H_2O\rightarrow2KOH+H_2\)
.......................y...........y..................y..........\(\frac{1}{2}\)y............
- Gọi số mol của Na, K trong hỗn hợp lần lượt là x, y ( x, y > 0 )
Ta có : \(m_{hh}=m_{Na}+m_K=n_{Na}.M_{Na}+n_K.M_K=8,5\)
=> \(23x+39y=8,5\) ( I )
\(n_{H_2}=\frac{V_{H_2}}{22,4}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
Mà \(n_{H_2}=n_{H_2\left(I\right)}+n_{H_2\left(II\right)}\)
=> \(0,5x+0,5y=0,15\left(II\right)\)
- Từ ( I ) và ( II ) ta có hệ phương trình : \(\left\{{}\begin{matrix}23x+39y=8,5\\0,5x+0,5y=0,15\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}23\left(0,3-y\right)+39y=8,5\\x=0,3-y\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}6,9-23y+39y=8,5\\x=0,3-y\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}y=0,1\\x=0,3-0,1=0,2\end{matrix}\right.\) ( TM )
=> \(\left\{{}\begin{matrix}n_{Na}=0,2\left(mol\right)\\n_K=0,1\left(mol\right)\end{matrix}\right.\)
-> \(m_{Na}=n.M=0,2.23=4,6\left(g\right)\)
Mà \(m_{hh}=m_{Na}+m_K=8,5\)
=> \(m_K=m_{hh}-m_{Na}=8,5-4,6=3,9\left(g\right)\)
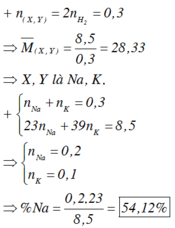
nH2=3,36/22,4=0,15(mol)
2X +2nH20 ---> 2X(oH)n+nH2
0,3/n 0,15
Ta có 0,3/n .X=10,1
----> X=36,7n
---> 2 kl kiềm là Na, K
nNa=nK=0,05
%mNa=\(\frac{0,15.23}{10,1}.100\%=34,15\%\)
%mK=100-34,15=65,85%