Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho hỗn hợp gồm N2, H2, NH3 đi qua dung dịch H2SO4 đặc, dư thì chỉ có NH3 phản ứng
2NH3+ H2SO4→ (NH4)2SO4
Sau phản ứng thể tích khí còn một nửa
→ %VNH3= 50%

gọi số mol N2 là xmol ,H2 là ymol
n khí = 22,4/22,4=1mol=>x + y =1(1)
theo bài ra hỗn hợp khí có tỉ khối với H2 là 3,6 nên ta có pt
x-4y=0(2)
từ (1) và (2) => x=0,8 mol : y=0,2 mol
=> mN2 = 0,8 * 14=11,2 g , mH2=0,2*2=0,2 g
=> m Khí = 11,2 + 0,4=11,6 g
=>%mN2=11,2*100/11,6=96,55%
=>%mH2=100-96,55=3,45%

Đáp án : C
FeO + 2HCl -> FeCl2 + H2O FeCl2 + 2NH3 + 2H2O -> Fe(OH)2 + 2NH4Cl 4Fe(OH)2 + O2 + 2H2O -> 4Fe(OH)3 2Fe(OH)3 -> Fe2O3 + 3H2O CuO + 2HCl -> CuCl2 + H2O
Số mol các oxide trong mỗi phần : nFeO = nFeCl2 = nFe(OH)2 = nFe(OH)3 = 2.nFe2O3 = 2.16/160 = 0,2 mol => nCuO = nCuCl2 = (30,4/2 - 0,2.72)/80 = 0,01 mol
CuCl2 (rắn) + H2SO4 (đ,n) -> 2HCl + CuSO4
0,01 -> 0,02 mol
6FeCl2 + 6H2SO4 -> 3SO2 + 6H2O + Fe2(SO4)3 + 4FeCl3
0,2 -> 0,1 mol
Cl- + H+ -> HCl
=> nHCl = 0,42 mol ; nSO2 = 0,1 mol Khi cho hỗn hợp khí và hơi gồm HCl, SO2 và H2O đi qua lượng dư P2O5 thì chỉ có H2O bị giữ lại, thể tích khí còn lại là : V = 22,4.(0,42 + 0,1) = 11,648 lit

Gọi hh khí ban đầu là X và hh khí sản phẩm là Y.
\(d_{\dfrac{X}{H_2}}=3,6\rightarrow M_X=3,6.2=7,2\left(\dfrac{g}{mol}\right)\)
Ta có:
\(\dfrac{n_{N_2}}{n_{H_2}}=\dfrac{7,2-2}{28-7,2}=\dfrac{5,2}{20,8}=\dfrac{1}{4}\) ( quy tắc đường chéo )
Gọi x là số mol N2 tham gia phản ứng.
PTHH:
\(N_2+3H_2\xrightarrow[Fe]{t^o}2NH_3\)
Trc p/ư: 1 4
p/ư: x 3x 2x (mol)
sau p/ư: 1-x 4-3x 2x
\(\rightarrow n_Y=1-x+4-3x+2x=5-2x\left(mol\right)\)
\(d_{\dfrac{Y}{H_2}}=4,5\rightarrow M_Y=4,5.2=9\left(\dfrac{g}{mol}\right)\)
BTKL: mX = mY
\(m_Y=1.28+4.2=36\left(g\right)\)
\(\rightarrow\dfrac{36}{9}=5-2x\)
\(\rightarrow x=0,5\)
Giả sử phản ứng xảy ra hoàn toàn:
\(\dfrac{1}{1}< \dfrac{4}{3}\) --> N2 hết, H2 dư.
Trước:
\(\%V_{N_2}=\dfrac{1.22,4}{5.22,4}.100\%=20\%\)
\(\%V_{H_2}=100\%-20\%=80\%\)
Sau:
\(\%V_{NH_3}=\dfrac{1.22,4}{4.22,4}.100\%=25\%\)
\(\%V_{N_2}=\dfrac{\left(1-0,5\right).22,4}{4.22,4}.100\%=12,5\left(\%\right)\)
\(\%V_{H_2}=\dfrac{\left(4-1,5\right).22,4}{4.22,4}.100\%=62,5\%\)

Cho hỗn hợp X qua dung dịch brom dư
thấy hỗn hợp X giảm đi 25% theo thể tích
⇒ nAnkadien = 25% nX
Cho hỗn hợp Y qua dung dịch brom,
thể tích hỗn hợp Y không giảm
⇒ Y gồm Ankan và H2 dư.
⇒ nH2 phản ứng = 2nAnkadien
= 50% nX
⇒ nY = nX – nH2 phản ứng
⇒ nY : nX = 1 : 2
Mà MY = 30 và mY = mX
⇒ MX = 15
Có MX = ( MAnkadien + 3 MH2 ) : 4
⇒ MAnkadien =54
⇒ Ankadien đó là C4H6.
Đáp án A.


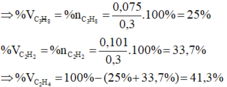
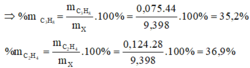
Khi cho hỗn hợp gồm N2, H2và NH3 đi qua dung dịch H2SO4 đặc, dư thì toàn bộ NH3 bị hấp thụ.
Theo giả thiết thì sau khi đi qua dung dịch H2SO4 đặc thì thể tích khí còn lại một nửa
\(\rightarrow\)Coi\(\text{ V(NH3 )=1}\) thì\(\text{ V(N2) +V(H2)=1 (1)}\)
\(\frac{\text{(1.17+VN2.28+VH2.2)}}{2}.100\%\)=8x2(2)
Giải (1) và (2) ta có \(\text{V (N2)=0,5, V(NH3)=0,5}\)
%N2=%VH2=\(\frac{0,5}{2}.100\%\)=25%
%NH3 =50%
hiểu chết liền