Ngâm một bản kẽm có khối lượng 50g trong dd CuSO4. Sau một thời gian phản ứng xong, lấy bản kẽm ra rửa nhẹ, sấy khô cân được 49,82g. Xác định lượng CuSO4có trong dung dịch.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Zn + CuSO4 -> ZnSO4 + Cu
Đặt nCu=a
Ta có:
65a-64a=50-49,82
=>a=0,18
Theo PTHH ta có:
nCuSO4=nCu=0,18(mol)
mCuSO4=160.0,18=28,8(g)
Gọi x là số mol Zn phản ứng
PTHH : Zn + CuSO4->ZnSO4+Cu
x-> x -> x (mol)
m(kim loại giảm)= 50-49,82=0,18(g)
mặt khác theo pt: m(kl giảm) =65x-64x
=> 65x-64x=0.18
=> x = 0,18(mol)
mCuSO4=0,18.160=28,8(g)

Gọi số mol Zn bị hòa tan là a (mol)
PTHH: Zn + FeSO4 --> ZnSO4 + Fe
______a---------------------------->a
=> 50 - 65a + 56a = 49,82
=> a = 0,02 (Mol)
=> mZn = 0,02.65 = 1,3(g)

Gọi x là số mol Zn p.ứ
Zn + CuSO4 = ZnSO4 + Cu
x x x (mol)
Vì khi phản ứng Zn tác dụng với CuSO4 và Cu bám trên bề mặt lá kẽm nên sau phản ứng ta thu được 49,82g khối lượng chất rắn gồm Zn dư và Cu
Ta có: 65x - 64x = 50 - 49,82 = 0,18(g)
=> x = 0,18 (mol)
Khối lượng CuSO4 trong dung dịch là
0,18 x 160 = 28,8 (g)

\(m_{ddCuCl_2}=1,2.300=360\left(g\right)\)
=> \(m_{CuCl_2}=\dfrac{360.20}{100}=72\left(g\right)\)
=> \(n_{CuCl_2}=\dfrac{72}{135}=\dfrac{8}{15}\left(mol\right)\)
PTHH: Zn + CuCl2 --> ZnCl2 + Cu
_____a----->a--------->a-------->a
=> 25 - 65a + 64a = 18
=> a = 7 (sai đề)

Đáp án C
nCuSO4 = 0,2. 0,5 = 0,1 (mol) ; Gọi nFe phản ứng = x (mol)
PTHH: Fe + CuSO4 → FeSO4 + Cu ↓
Theo PTHH 56x 64x
Khối lượng kim loại tăng ∆ = (64x -56x)= 8x (g)
Theo đề bài ∆m tăng = ( 100,4 -100) = 0,4 (g)
=> 8x = 0,4
=> x = 0,05 (mol)
=> mFeSO4 = 0,05. 152 = 7,6 (g)

Đáp án C
Ta cớ pứ: Fe + Cu2+ → Fe2+ + Cu.
Đặt nFepứ = a ⇒ nCu = a.
⇒ mCu – mFe pứ = 0,4 Û 8a = 0,8 Û a = 0,05.
⇒ mFeSO4 = 0,05×152 = 7,6 gam
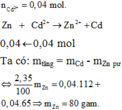
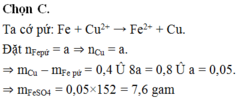
Zn+CuSO4--->ZnSO4+Cu
Đặt nCu=a
Ta có:
65a-64a=50-49,82
=>a=0,18
Theo PTHH ta có:
nCuSO4=nCu=0,18(mol)
mCuSO4=160.0,18=28,8(g).
Gọi n Cu sau phản ứng là x
PTHH:Zn+CuSO4---->ZnSO4+Cu
--------x------x-------------x----------x
m Zn=65x , m Cu=64x
Khối lượng KL giảm suy ra
m Zn- m Cu=50-49,82
=> 65x-54x=0,18
=>x=0,18
m CuSO4= 0,18.160=28,8(g)