Cho 4,48 lít khí N2 (đktc) tác dụng với H2 dư thu được 1,7 gam NH3. tính H% PHẢN ỨNG
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{N_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(N_2+3H_2\underrightarrow{t^o}2NH_3\)
Theo PT: \(n_{NH_3\left(LT\right)}=2n_{N_2}=0,4\left(mol\right)\)
\(\Rightarrow m_{NH_3\left(LT\right)}=0,4.17=6,8\left(g\right)\)
\(\Rightarrow H=\dfrac{1,7}{6,8}.100\%=25\%\)

$n_{N_2} = 0,4(mol) ; n_{H_2} = 0,9(mol) ; n_{NH_3} = 0,2(mol)$
$N_2 + 3H_2 \buildrel{xt,t^,p}\over\rightleftharpoons 2NH_3$
Ta thấy :
$n_{N_2} : 1 > n_{H_2} : 3$ do đó hiệu suất tính theo số mol Hidro
$n_{H_2\ pư} = \dfrac{3}{2}n_{NH_3} = 0,3(mol)$
$H = \dfrac{0,3}{0,9}.100\% = 33,33\%$

Đáp án C
Cho Ag thu được tác dụng với HNO3 đặc nóng dư thu được 0,145 mol khí NO2.
→ n A g = 0,145
Ta có: M X < 112
Nếu X là HCHO thì n x = 0 , 126875 → n A g = 0 , 5075 (loại).
Gọi x là số nhóm CHO trong X → n x = 0 , 145 2 x → M x = 56 x
thỏa mãn x=1 thì X là CH2=CH-CHO
→ m = 4,06 + 0,145.2 = 4,35 gam

Đáp án C
Cho Ag thu được tác dụng với HNO3 đặc nóng dư thu được 0,145 mol khí NO2


Giải thích: Đáp án C
Cho Ag thu được tác dụng với HNO3 đặc nóng dư thu được 0,145 mol khí NO2.
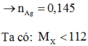
Nếu X là HCHO thì ![]()
Gọi x là số nhóm CHO trong X ![]()
thỏa mãn x=1 thì X là CH2=CH-CHO
![]()

Chọn A
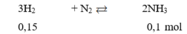
Do hiệu suất phản ứng là 80% nên thể tích H 2 cần dùng là:
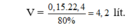

N2 + 3H2 \(\overset{t^o,p,xt}{⇌}\) 2NH3.
Cứ 1 lít N2 tác dụng với 3 lít H2 tạo ra 2 lít NH3. Vậy a lít N2 tác dụng với 3a lít H2 tạo ra 2a lít NH3, thu được (5-a)+(5-3a)+2a=7 (lít), suy ra a=1,5 (lít).
Thể tích mỗi khí trong hỗn hợp X gồm khí N2 (5-1,5=3,5 (lít)), khí H2 (5-3.1,5=0,5 (lít)) và khí NH3 (2.1,5=3 (lít)).
Hiệu suất phản ứng là H=(5-0,5)/5.100%=90% (hiệu suất tính theo H2 do H2 thiếu).
nN2 = 4.48/22.4=0.2 mol
nNH3 = 1.7/17 = 0.1 mol
N2 + 4H2 -to-> 2NH3
0.05___________0.1
%H = 0.05/0.2*100% = 25%