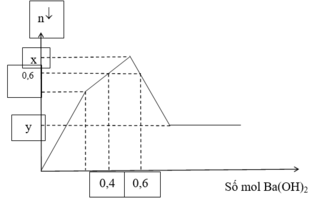
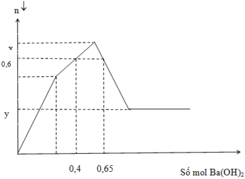
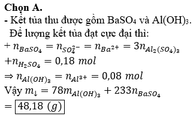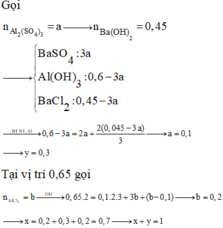dung dịch x chứa 19,77g hỗn hợp alcl3 và al2(so4)3 phản ứng hòa toàn với ba(oh)2 thu được kết tủa cực đại và 44,34g và tính mol mỗi chất trong x
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


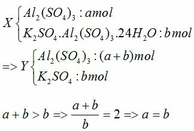
Vì dung dịch sau phản ứng chỉ chứa một chất tan => Z chỉ chứa KAlO2 hoặc K2SO4.
Khi cho từ từ Ba(OH)2 vào Y thì có thể xảy ra các phản ứng:
Al2(SO4)3 + 3Ba(OH)2 → 2Al(OH)3 + 3BaSO4(1)
2b → 6b 4b 6b (mol)
K2SO4 + Ba(OH)2 → 2KOH + BaSO4 (2)
b → b 2b b (mol)
Al(OH)3 + KOH → KAlO2 + 2H2O (3)
2b →2b 2b (mol)
· Trường hợp 1: Chất tan trong Z là K2SO4 → vừa đủ phản ứng (1)
Theo đề => a= b = 0,02 mol
nBaSO4 = nBa(OH)2 = 6b = 0,12mol
nAl(OH)3 = 4b = 0,08mol
m1= 948 . 0,02 + 342 . 0,02 = 25,8 gam
m2 = 0,08 . 78 + 0,12 . 233 = 34,2 gam
V = 0,12/2 = 0,06 lít = 60ml
· Trường hợp 2: Chất tan trong Z là KAlO2 →xảy ra cả (1,2,3)
nKAlO2 = 0,02mol
=> 2b = 0,02 => a = b =0,01
nBaSO4 = nBa(OH)2 = 7b = 0,07
nAl(OH)3 = 4b – 2b = 0,02
=> m1= 948.0,01 + 342.0,01 = 12,9 gam
m2 = 0,02.78 + 0,07.233 = 17,87 gam
V = 0,07/2 = 0,035 lít = 35ml

Chọn đáp án C
Nếu Al(OH)3 đã bị hòa tan
⇒
nOH- từ m1 gam rắn ![]()
Mà
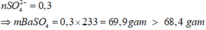
⇒ Al(OH)3 không bị hòa tan và Y còn Al3+ dư ⇒ Y là dung dịch Al2(SO4)3
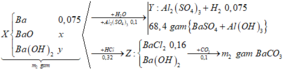
Từ tỉ lệ phản ứng: 3Ba(OH)2 + Al2(SO4)3 ⇒ nBaSO4 : nAl(OH)3 = 3 : 2 ⇒ Đặt là 3a và 2a
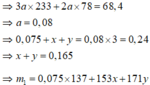
⇒
![]()
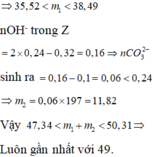

Đáp án D
• 0,42 mol NaOH + 0,02 mol Fe2(SO4)3; 0,04 mol Al2(SO4)3 → 500ml X + ↓
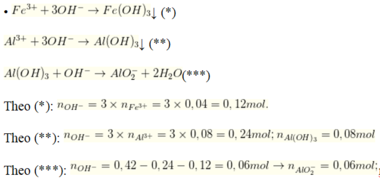
nAl(OH)3 = 0,08 - 0,06 = 0,02 mol
Vậy sau phản ứng 500ml dung dịch X gồm 0,06 mol Na[Al(OH)4]; 0,18 mol Na2SO4
→ CM các chất trong X là CMNa2SO4 = 0,06 : 0,5 = 0,12 M;
CMNa[Al(OH)4] = 0,18 : 0,5 = 0,36 M

Đáp án D
Đặt số mol Al2(SO4)3 là x; AlCl3 là 3x
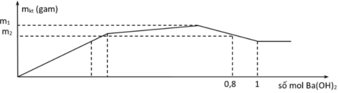
Khi đường kết tủa đi ngang, là khi Al(OH)3 tan hoàn toàn, tạo thành Al(OH)4− và lúc đó chỉ còn BaSO4
nOH− = 4.(2x + 3x) = 1.2 → x = 0,1 mol
Khi kết tủa cực đại, nOH− = 3.(2x+3x) = 1,5 mol:
→ n Ba ( OH ) 2 = 0,75 mol → m m a x = 233.0,1.3 + 0,5.78 = 108,9 = m 1
Tại n B a ( O H ) 2 =0,8 mol → n O H - = 1,6 mol lúc này kết tủa Al(OH)3đã bị tan ra, mBaSO4 đạt cực đại:
→ mmax = 233.0,1.3 +(0,5.4-1,6).78 = 101,1 = m2