Nguyên tố Agon có ba loại đồng vị có số khối bằng 36,38 và A.Phần trăm số nguyên tử ứng của ba đồng vị lần lượt bằng 0,34%,0,06%,99,6%.Biết 125 nguyên tử có khối lượng bằng 4997,5 đvc .Tính khối lượng nguyên tử trung bình của Ar và số khối của đồng vị thứ 3.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A.
Nguyên tử khối trung bình của Ar: 4997,5:125=39.98(u)
Ta có phương trình:
A = 0 , 34 . 36 + 0 , 06 . 38 + 99 , 6 . A 100 = 39 , 98 ⇒ A = 40 ( u )

\(A_{tb}=\frac{36.0,34+38.0,06+39.99,6}{100}=\text{38,9892}\)

Đáp án D
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
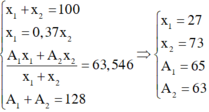

Đáp án B
Chọn số lượng nguyên tử Y là 100 thì số lượng nguyên tử X là 37.
Gọi số khối của X là A thì số khối của Y là (128 – A).
Do đó nguyên tử khối trung bình của Cu là:
M ¯ = 37 A + 100 ( 128 - A ) 37 + 100 = 63 , 54 ⇔ A = 65
Vậy số khối của X và Y lần lượt là 65 và 63.
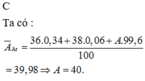


\(\overline{A_{Ar}}=\frac{36\times0.34+38\times0.06+A\times99.6}{100}=39.98\)
\(\Leftrightarrow A=40\)