Câu 1: Một hh nặng 51,6g gồm các oxit kim loại là FeO, Al2O3, CuO. Khử hoàn toàn hh này bằng H2 ở nhiệt độ cao thì thu được 45,2g hh chất rắn Y. CHo chất răn Y vào dd HCl dư thì thu được Vlits khí H2(đktc) và 19,2g chất răn skhoong tan. Xác định V và % về khối lượng các oxit trong hh ban đầu?
Câu 2: Cho 41g hh gồm Zn, Cu, Ag nhúng vào dd h2so4 loãng dư thì thấy khối lượng chất rắn tăng lên 2,4g. xác định % về khối lượng các kim loại trong hh ban đầu
Câu 3: khử hoàn toàn 80,3g hh X gồm ZnO, Fe2O3, CuO bằng H2 ở nhiệt độ cao thì thu được 61,1g chất rắn. Nếu hòa tan 20,075g hh X bằng dd H2SO4 thì thu được bao nhiêu gam muối?

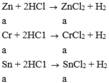
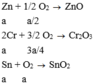
C1: Đặt:
nFeO = x mol
nAl2O3= y mol
nCuO = z mol
mhh= 72x + 102y + 80z = 51.6g (1)
- Khử hoàn toàn hh :
FeO + H2 -to-> Fe + H2O
x____________x
CuO + H2 -to-> Cu + H2O
z_____________z
hh rắn Y : Fe, Cu, Al2O3
mY= 56x + 102y + 64z = 45.2g (2)
- Cho hh Y vào dd HCl dư :
Fe + 2HCl --> FeCl2 + H2
x__________________x
Al2O3 + 6HCl --> 2AlCl3 + 3H2O
Chất rắn không tan : Cu
nCu = 19.2/64=0.3 mol
=> 0x + 0y + z = 0.3 (3)
Giải (1), (2) và (3) :
x= 0.1
y= 0.2
z= 0.3
VH2= 0.1*22.4=2.24l
mFeO = 7.2g
mAl2O3= 20.4g
mCuO= 0.3*80=24g
%FeO= 13.95%
%Al2O3= 39.53%
%CuO = 46.52%