Cho 1.67gam hỗn hợp gồm 2 kim loại ở 2 chu kỳ liên tiếp nhau thuộc nhóm IIA tác dụng hết với dung dịch HCl(dư), thoát ra 0.672 lít khí H2(ở đktc).Tìm 2 kim loại đó(Mg=24, Ca=40, Sr=87, Ba=137)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Kim loại nhóm IIA, có mức oxi hóa = +2 trong hợp chất
nH2 = 0,03 mol
Gọi X là kí hiệu chung của 2 kim loại
X + 2HCl → XCl2 + H2
0,03 ← 0,03 (mol)
⇒ M = 55,6
MCa = 40 < 55,67 < MSr = 88

Gọi nguyên tử khối trung bình của 2 kim loại cần tìm là R
\(R+2HCl\rightarrow RCl_2+H_2\\ n_R=n_{H_2}=0,075\left(mol\right)\\ \Rightarrow M_R=\dfrac{2,2}{0,075}=29,33\\ \Rightarrow2kimloạicầntìmlà:Mg,Ca\)

\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi M là hh 2 kim loại ở 2 chu kì liên tiếp
\(M+2HCl\rightarrow MCl_2+H_2\)
\(n_M=n_{H2}=0,15\left(mol\right)\)
\(M_M=\dfrac{4,4}{0,15}=29,33\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow M_{Mg}=24< 29,33< M_{Ca}=40\)
Vậy 2 kim loại cần tìm là Mg va Ca

Đáp án B.
Gọi công thức chung của hai kim loại là X
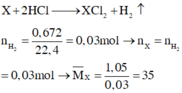
Mà hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA → 2 kim loại đó là Ca và Mg



nH2 = 0.03 (mol)
Gọi A , B là 2 kim loại cần tìm ( hóa trị II)
R là CTC của 2 kim loại ( MA < MR < MB )
PT : R + 2HCl → RCl2 + H2↑
Mol : 0,03 <----------------0,03
=> MR = \(\frac{1,67}{0,03}=55,67\)
Do 2 kim loại ở 2 chu kì liên tiếp nhau thuộc nhóm IIA => A,B lần lượt là Ca và Cr
thay Cr = Sr