Hòa tan hoàn toàn 5 g CaCO3 trong 40 ml dung dịch HCl sau Phản ứng phải dùng hết 20 ml dung dịch NaOH Để trung hòa lượng axit dư Mặt khác 50 ml dung dịch HCl phản ứng vừa đủ với 150 ml dung dịch NaOH tính nồng độ mol của dung dịch HCl và NaOH
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án D
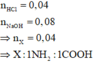
(Hoặc có thể nhìn vào đáp án suy ra X có 1 nhóm COOH)
Gọi CTCT X: H_2NRCOOH
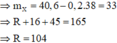
Chọn B hoặc D. Do X là một α-amino axit nên chọn D

Đáp án C
nCaCO3 = 20: 100 = 0,2 mol
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Mol: 0,2 → 0,2
nNaOH = 0,1.2,5 = 0,25 mol
Ta thấy: nCO2 < nNaOH < 2nCO2 => phản ứng tạo hỗn hợp muối NaHCO3 và Na2CO3

Chọn đáp án D.
► Xét thí nghiệm 1:
Quy quá trình về: X + 0,04 mol HCl + 0,08 mol NaOH.
⇒ nX = 0,08 – 0,04 = 0,04 mol
⇒ 250 ml dung dịch X chứa 0,2 mol H2RCOOH.
⇒ Mmuối = 35 ÷ 0,2 = 175 (H2NRCOOK)
⇒ R = 76 (-C6H4-)

Chọn đáp án D
► Xét thí nghiệm 1: Quy quá trình về: X + 0,04 mol HCl + 0,08 mol NaOH.
⇒ nX = 0,08 – 0,04 = 0,04 mol ⇒ 250 ml dung dịch X chứa 0,2 mol H2RCOOH.
||⇒ Mmuối = 35 ÷ 0,2 = 175 (H2NRCOOK) ⇒ R = 76 (-C6H4-) ⇒ chọn D.

n HCl = 0,8.1,5 = 1,2(mol)
n HCl dư = n NaOH = 0,2.1 = 0,2(mol)
=> n HCl pư = 1,2 - 0,2 = 1(mol)
$2H^+ + O^{2-} \to H_2O$
n O(oxit) = 1/2 n HCl = 0,5(mol)
m Fe + m O = m oxit
=> n Fe = (29 - 0,5.16)/56 = 0,375(mol)
Ta có :
n Fe / n O = 0,375 / 0,5 = 3 / 4 nên oxit là Fe3O4

Số mol H 2 S O 4 trong 100ml dung dịch 0,5M là :
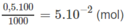
Số mol NaOH trong 33,4 ml nồng độ 1M :
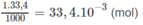
H 2 S O 4 + 2NaOH → N a 2 S O 4 + 2 H 2 O
Lượng H 2 S O 4 đã phản ứng với NaOH :

Số mol H 2 S O 4 đã phản ứng với kim loại là :
5. 10 - 2 - 1.67. 10 - 2 = 3,33. 10 - 2 mol
Dung dịch H 2 S O 4 0,5M là dung dịch loãng nên :
X + H 2 S O 4 → X S O 4 + H 2 ↑
Số mol X và số mol H 2 S O 4 phản ứng bằng nhau, nên :
3,33. 10 - 2 mol X có khối lượng 0,8 g
1 mol X có khối lượng: 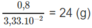
⇒ Mkim loại = 24 g/mol.
Vậy kim loại hoá trị II là magie.

