2/ Cho 20 gam CaCO3tác dụng với 91,25 gam dung dịch HC1 20%. Tính thể tích
khí CO2 thoát ra ở đktc và nồng độ % các chất trong dung dịch thu được
3/ Cho 39,4 gam BaCO3tác dụng với 73 gam dung dịch HC1 25%. Tính thể tích
khí CO2 thoát ra ở đktc và nống độ % các chất trong dung dịch thu được
4/ Cho 30 gam CaCO3tác dụng với 91,25 gam dung dịch HC1 20%. Tính thể tích
khí CO2 thoát ra ở đktc và nồng độ % các chất trong dung dịch thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
Ta lại có: \(C_{\%_{HCl}}=\dfrac{m_{HCl}}{91,25}.100\%=20\%\)
=> mHCl = 18,25 (g)
=> \(n_{HCl}=\dfrac{18,25}{36,5}=0,2\left(mol\right)\)
PTHH: CaCO3 + 2HCl ---> CaCl2 + H2O + CO2↑
Ta thấy: \(\dfrac{0,2}{1}>\dfrac{0,2}{2}\)
Vậy CaCO3 dư
Theo PT: \(n_{CO_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(V_{CO_2}=0,1.22,4=2,24\left(lít\right)\)
Theo PT: \(n_{H_2O}=n_{CaCl_2}=n_{H_2O}=0,1\left(mol\right)\)
=> \(m_{CaCl_2}=0,1.111=11,1\left(g\right)\)
\(m_{H_2O}=0,1.18=1,8\left(g\right)\)
=> \(m_{dd_{CaCl_2}}=20+91,25-1,8-\left(44.0,1\right)=105,05\left(g\right)\)
=> \(C_{\%_{CaCl_2}}=\dfrac{11,1}{105,05}.100\%=10,57\%\)
Ta có: \(m_{dd_{H_2O}}=20+91,25-11,1-\left(44.0,1\right)=95,75\left(g\right)\)
=> \(C_{\%_{H_2O}}=\dfrac{1,8}{95,75}.100\%=1,88\%\)

Bài 4 :
\(n_{CaCO3}=\dfrac{30}{100}=0,3\left(mol\right)\)
\(m_{ct}=\dfrac{20.91,25}{100}=18,25\left(g\right)\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
Pt : \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O|\)
1 2 1 1 1
0,3 0,5 0,25 0,25
Lập tỉ số so sánh : \(\dfrac{0,3}{1}>\dfrac{0,5}{2}\)
⇒ CaCO3 dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
\(n_{CO2}=\dfrac{0,5.1}{2}=0,25\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,25.22,4=5,6\left(l\right)\)
\(n_{CaCl2}=\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
⇒ \(m_{CaCl2}=0,25.111=27,75\left(g\right)\)
\(m_{ddspu}=30+91,25-\left(0,25.44\right)=110,25\left(g\right)\)
\(C_{CaCl2}=\dfrac{27,75.100}{110,25}=25,17\)0/0
Chúc bạn học tốt

Chọn đáp án D
Đặt n M 2 C O 3 = x ; n M H C O 3 = y ; n M C l = z ⇒ n H C l p h ả n ứ n g = 2 x + y
Bảo toàn nguyên tố Clo: n A g C l = 0 , 7 = 2 x + y + z ; n C O 2 = 0 , 4 = x + y
![]()
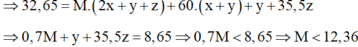
⇒ M là Liti ⇒ M = 7 ⇒ giải hệ có: x = y = 0,2 mol; z = 0,1 mol.
![]()

Chọn C
m2 gam X có thể phản ứng với HC1 tạo H2 Þ Có Al dư Þ nAl dư = 0,03/1,5 = 0,02
Vì AI dư Þ Toàn bộ Ag+ và Cu2+ đã bị khử hết về kim loại đơn chất
BTE Þ 3nAl phản ứng = 0,03x2 + 0,03 = 0,09 Þ nAl phản ứng = 0,03
Vậy m1 = (0,03 + 0,02)x27 = 1,35; m2 = 0,02x27 + 0,03x64 + 0,03x108 = 5,7

mNaOH=11(g) -> nNaOH= 0,275(mol)
mH3PO4=9,8(g) -> nH3PO4=0,1(mol)
Ta có: 2< nNaOH/nH3PO4 = 0,275/0,1=2,75< 3
=> P.ứ kết thúc thu được hỗn hợp dd Na3PO4 và Na2HPO4
PTHH: 3 NaOH + H3PO4 -> Na3PO4 + 3 H2O
3x_____________x________x(mol)
2 NaOH + H3PO4 -> Na2HPO4 +2 H2O
2y_____y__________y(mol)
mddX=55+24,5=79,5(g)
\(\left\{{}\begin{matrix}3x+2y=0,275\\x+y=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,075\\y=0,025\end{matrix}\right.\)
=> mNa3PO4=0,075.164=12,3(g)
mNa2HPO4=142.0,025=3,55(g)
=>C%ddNa3PO4=(12,3/79,5).100=15,472%
C%ddNa2HPO4=(3,55/79,5).100=4,465%
Ta có: \(\left\{{}\begin{matrix}n_{NaOH}=\dfrac{55\cdot20\%}{40}=0,275\left(mol\right)\\n_{H_3PO_4}=\dfrac{24,5\cdot40\%}{98}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo HPO42- và PO43-
PTHH: \(2NaOH+H_3PO_4\rightarrow Na_2HPO_4+2H_2O\)
2a_______a___________a_______2a (mol)
\(3NaOH+H_3PO_4\rightarrow Na_3PO_4+3H_2O\)
3b_______b_________b______3b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}2a+3b=0,275\\a+b=0,1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,025\\b=0,075\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Na_2HPO_4}=\dfrac{0,025\cdot142}{55+24,5}\cdot100\%\approx4,47\%\\C\%_{Na_3PO_4}=\dfrac{0,075\cdot164}{55+24,5}\cdot100\%\approx15,47\%\end{matrix}\right.\)


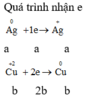


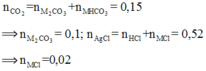
Bài 2 :
\(n_{CaCO3}=\dfrac{20}{100}=0,2\left(mol\right)\)
\(m_{ct}=\dfrac{20.91,25}{100}=18,25\left(g\right)\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
Pt : \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O|\)
1 2 1 1 1
0,2 0,5 0,2 0,2
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
⇒ CaCO3 phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của CaCO3
\(n_{CO2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
\(n_{CaCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{CaCl2}=0,2.111=22,2\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,5-\left(0,2.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddspu}=20+91,25-\left(0,2.44\right)=102,45\left(g\right)\)
\(C_{CaCl2}=\dfrac{22,2.100}{102,45}=21,67\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{3,65.100}{102,45}=3,56\)0/0
Chúc bạn học tốt