hòa tan 13,8g muối cacbonat của kim loại hóa trị 1 trong dung dịch chứa 0,22 mol HCl. Sau khi phản ứng kết thúc thu được dung dịch A và 6,72l khí(đktc).
a)Axit H2SO4 phản ứng hết hay dư.
b)Tính tổng khối lượng muối có trong dung dịch A.
c)lượng H2 thu được ở trên cho đi qua bột sắt từ oxit nung nóng để khử hoàn toàn thu đc m(g) sắt với hiệu suất 80%.tính m??
(đang cần gấp)

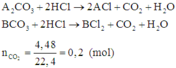
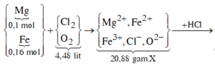
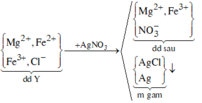
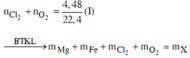
hòa tan 13,8g muối cacbonat của kim loại hóa trị 1 trong dung dịch chứa 0,22 mol HCl. Sau khi phản ứng kết thúc thu được dung dịch A và 6,72l khí(đktc).
a)Axit H2SO4 phản ứng hết hay dư.
b)Tính tổng khối lượng muối có trong dung dịch A.