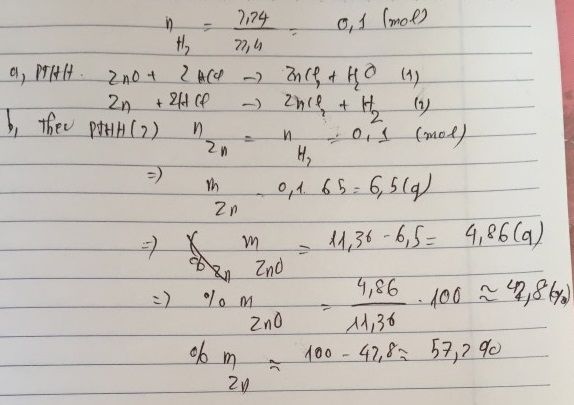hòa tan hoàn toàn hỗn hợp A gồm Zn , ZnO phải dùng hết 448ml dd HCl 3,65% (d = 1,12 g/ml) thu được dd B và 2,24 lít khí thoát ra ở đktc. Tính thành phần phần trăm về khối lượng của mỗi chất trong hỗn hơp A?
(giúp mk bài này với ạ, mình đang cần gấp, cảm ơn ạ)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{HCl} = \dfrac{448.1,12.3,65\%}{36,5} = 0,50176(mol)\\ Zn + 2HCl \to ZnCl_2 + H_2\\ ZnO + 2HCl \to ZnCl_2 + H_2O\\ n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ n_{ZnO} = \dfrac{n_{HCl} - 2n_{Zn}}{2} = \dfrac{0,50176-0,1.2}{2} = 0,15088(mol)\\ \%m_{Zn} = \dfrac{0,1.65}{0,1.65 + 0,15088.81}.100\% = 34,72\%\\ \%m_{ZnO} = 65,28\%\)

pthh: Zn+HCl→ZnCl2+H2 (1)
ZnO+HCl→ZnCl2+H2O (2)
theo bài ra số mol của H2=0,2 (mol)
theo pt1 ta có nZn=nH2=0,2 (mol)
⇒ mZn=0,2 .65=13 (g)→mZnO=21,1-13=8,1 (g) →nZnO=0,1 (mol)
%Zn=13.100%/21,1=61,61%
%ZnO=38,39%
Theo pt 1 nHCl=2nZn=0,4(mol) (3)
Theo pt2 nHCl=2nZnO=0,4 (mol) (4)
Từ 3,4 ⇒nHCl=0,8 (mol)
V HCl=0,4 (lít)=400ml

C32:
a, \(n_C=\dfrac{2,4}{12}=0,2\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_{CO_2}=n_C=0,2\left(mol\right)\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{NaOH}=0,3.1=0,3\left(mol\right)\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{CO_2}}=1,5\) → Pư tạo NaHCO3 và Na2CO3
PT: \(CO_2+NaOH\rightarrow NaHCO_3\)
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=n_{NaHCO_3}+n_{Na_2CO_3}=0,2\\n_{NaOH}=n_{NaHCO_3}+2n_{Na_2CO_3}=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NaHCO_3}=0,1\left(mol\right)\\n_{Na_2CO_3}=0,1\left(mol\right)\end{matrix}\right.\)
⇒ mNaHCO3 = 0,1.84 = 8,4 (g)
mNa2CO3 = 0,1.106 = 10,6 (g)
c, \(C_{M_{NaHCO_3}}=C_{M_{Na_2CO_3}}=\dfrac{0,1}{0,3}=\dfrac{1}{3}\left(M\right)\)
Lần sau bạn đăng tách câu hỏi ra nhé.
C31:
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
b, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{14,6}.100\%\approx44,52\%\\\%m_{ZnO}\approx55,48\%\end{matrix}\right.\)
c, \(n_{ZnO}=\dfrac{14,6-0,1.65}{81}=0,1\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Zn}+2n_{ZnO}=0,4\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,4.36,5}{10\%}=146\left(g\right)\)

a) $Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
b)
Theo PTHH : $n_{Zn} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$m_{Zn} = 0,2.65 = 13(gam)$
$m_{ZnO} = 21,1 - 13 = 8,1(gam)$
c) $n_{ZnO} = 0,1(mol)$
Theo PTHH : $n_{HCl} = 2n_{Zn} + 2n_{ZnO} = 0,6(mol)$
$m_{dd\ HCl} = \dfrac{0,6.36,5}{16,6\%} = 132(gam)$
d) $m_{dd\ sau\ pư} = 21,1 + 132 - 0,2.2 = 152,7(gam)$
$n_{ZnCl_2} = n_{Zn} + n_{ZnO} = 0,3(mol)$
$C\%_{ZnCl_2} = \dfrac{0,3.136}{152,7}.100\% = 26,72\%$

Fe + 2HCl -> FeCl2 + H2
0.2 0.1
FeO + 2HCl -> FeCl2 + H2O
0.1 0.2
a.\(nH2=\dfrac{2.24}{22.4}=0.1mol\)
\(\%mFe=\dfrac{0.1\times56\times100}{12.8}=43.8\%\)
\(\%mFeO=100-43.8=56.2\%\)
b.\(nFeO=\dfrac{12.8-\left(0.1\times56\right)}{56+16}=0.1mol\)
\(V_{HCl}=\dfrac{0.2+0.2}{2}=0.2l\)

Tiếp bài của creeper nhé:
c. Ta có: \(n_{ZnO}=\dfrac{4,86}{81}=0,06\left(mol\right)\)
Theo PT(1): \(n_{HCl}=2.n_{ZnO}=2.0,06=0,12\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{Zn}=2.0,1=0,2\left(mol\right)\)
=> \(n_{HCl}=0,12+0,2=0,32\left(mol\right)\)
=> \(m_{HCl}=0,32.36,5=11,68\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{11,68}{m_{dd_{HCl}}}.100\%=12\%\)
=> \(m_{dd_{HCl}}=\dfrac{292}{3}\left(g\right)\)
Theo đề, ta có:
\(D=\dfrac{\dfrac{292}{3}}{V_{dd_{HCl}}}=1,2\)(g/ml)
=> \(V_{dd_{HCl}}=81,1\left(ml\right)\)

PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
a, Ta có: \(n_{H_2}=0,1\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,1.24=2,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{2,4}{4,4}.100\%\approx54,55\%\\\%m_{MgO}\approx45,45\%\end{matrix}\right.\)
b, Ta có: mMgO = mhhA - mMg = 2 (g)
\(\Rightarrow n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{MgO}=0,1\left(mol\right)\)
\(\Rightarrow V_{HCl}=\dfrac{0,1}{2}=0,05\left(l\right)=50\left(ml\right)\)
Bạn tham khảo nhé!

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1=n_{Zn}\\ n_{ZnO}=\dfrac{14,6-6,5}{81}=0,1mol\\ C\%=\dfrac{0,2\cdot136}{175,6+14,6-0,2}=14,32\%\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\\ a)Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
\(b)m_{Zn}=0,1.65=6,5g\\ m_{ZnO}=14,6-6,5=8,1g\\ c)n_{ZnO}=\dfrac{8,1}{81}=0,1mol\\ ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
0,1 0,2
\(m_{ddHCl}=\dfrac{\left(0,2+0,2\right)36,5}{14,6}\cdot100=100g\)