Oxi hóa chậm m gam Fe ngoài không khí thu được 3 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3 và Fe dư. Hòa tan A vừa đủ bởi 200 ml dung dịch HNO3 thu được 0,56 lít khí NO duy nhất (đktc). Tính m và nồng độ mol/l của dung dịch HNO3?
https://hoc247.net/cau-hoi-oxi-hoa-cham-m-gam-fe-ngoai-khong-khi-thu-duoc-3-gam-hon-hop-a-gom-feo-fe3o4-fe2o3-va-fe-du-4601.html
Cho hỏi dòng thứ 5 sao 0.025.3/2 vậy ?
Còn dòng 6 nữa sao tính đc mfe2o3=3.6 rồi sao từ đấy suy ra mFe bđ

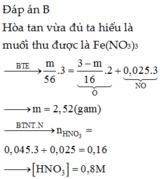
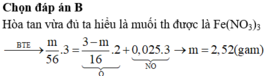
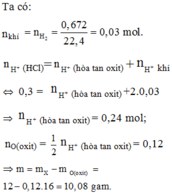
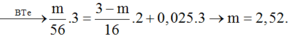
bạn để link như vậy thì khó tìm lắm mk làm cách khác đc ko
\(Fe+\left[O\right]\rightarrow A\)
\(A+HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+H_2O\)
\(n_{NO}=0.025\left(mol\right)\)
BTKL ta có: \(56n_{Fe}+16n_O=3\)
BT(e) ta có: \(3n_{Fe}-2n_O=3n_{NO}=0.075\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0.045\left(mol\right)\\n_O=0.03\left(mol\right)\end{matrix}\right.\)
\(n_{Fe\left(NO_3\right)_3}=n_{Fe}=0.045\left(mol\right)\)
Do HNO3 vừa đủ nên \(n_{HNO_3}=0.045\cdot3+0.025=0.16\)
CM(HNO3)=\(\frac{0.16}{0.2}=0.8\left(M\right)\)