1/ Hòa tan 15,80 gam hỗn hợp Al, Mg và Fe vào 500,0 ml dung dịch HCl 2,50 mol/l thu được 13,44 lít H2 ( đo ở đktc) và dung dịch A. Trong hỗn hợp có số mol Al bằng số mol Mg. Tính % khối lượng mỗi kim loại trong hỗn hợp đã hòa tan và tính khối lượng muối có trong dung dịch A.
2/ hòa tan hoàn toàn 12,8 gam hỗn hợp gồm Fe và FeO trong 500,0 ml dung dịch axit HCl vừa đủ thu được dung dịch A và 2,24 lít khí ( đo ở đktc). Tính nồng độ dung dịch HCl đã dùng và tính thể tích dung dịch axit HCl 2,00 mol/l cần lấy để pha được 500,0 ml dung dịch axit trên.
3/ Hòa tan hoàn toàn 7,8 hỗn hợp Mg và Al vào dung dịch HCl thì thu được 8,96 lít khí Hidro (đktc)
a) Tính % khối lượng mỗi kim loại trong hỗn hợp;
b) Khi cô cạn dung dịch sau phản ứng thu được bao nhiêu gam muối khan?


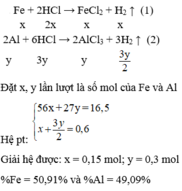
Bài 3:
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Gọi x, y lần lượt là số mol của Mg, Al
PTHH:
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
...x.............................x.............x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
..y.............................y...........1,5y
Ta có hệ PT: \(\left\{{}\begin{matrix}24x+27y=7,8\\x+1,5y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> \(m_{Mg}=0,1.24=2,4\left(g\right)\)
a. => \(\%Mg=\dfrac{2,4}{7,8}.100\%=30,77\%\)
=> \(\%Al=100\%-30,76\%=69,23\%\)
b. \(m_{MgCl_2}=0,1.95=9,5\left(g\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
\(\Rightarrow m_{muoi-khan}=9,5+26,7=36,2\left(g\right)\)
siêng v~ hôm nào t bí Hóa thì giúp t nhé ^^