(Bài 6 - Phần 4) : Hòa tan hoàn toàn x(g) hỗn hợp X gồm Fe, kim loại M(m), A(a) trong hỗn hợp H2SO4 loãng vừa đủ được 15,68(l) khí H2 ở ĐKTC và dung dịch C. Cô cạn dung dịch C, sấy khô được 82,9(g) muối khan. Tìm x.
(Bài 7 - Phần 4) : Trộn lẫn 700ml dung dịch H2SO4 60% (d=1,530 g/ml) với 500 ml dung dịch H2SO4 20% (d=1,143 g/ml) sau đó thêm một lượng nước cất vào, thu được dung dịch A. Khi cho Zn dư vào 200ml A thu được 2000ml khí H2 ở ĐKTC. Tính VddA.
(Bài 4 - Phần 5) : M là dung dịch chứa 0,8 mol HCl. N là dung dịch chứa hỗn hợp 0,2 mol Na2CO3 và 0,5 mol NaHCO3. Thực hiện 3 thí nghiệm:
Thí nghiệm 1 - Đổ rất từ từ M vào N.
Thí nghiệm 2 - Đổ rất thừ từ N vào M.
Thí nghiệm 3 - Đổ và trộn nhanh 2 dung dịch M và N.
Tính VCO2 sinh ra ở mỗi thí nghiệm?
(Bài 6 - Phần 5) : Có 500g dung dịch muối M(HCO3)n 6,478%. Thêm từ từ dung dịch H2SO4 đến khi thoát hết khí, sau đó đem cô cạn cẩn thận dung dịch thu được thấy được 27,06 (g) muối sunfat. Tìm công thức của muối cacbonat trên.

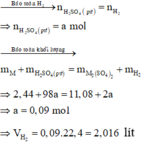
Bài 4
TN1: CO32- + H+ -----> HCO3-
0.2.......0.2..............0.2
HCO32-+ H+------> CO2↑+ H2O
0.6.........0.6.............0.6
=>VCO2=0.6*22.4=13.44 lít
TN2: CO32- + 2H+ -----> CO2↑+ H2O
0.2..........0.4..............0.2
HCO3- + H+ ------> CO2↑+ H2O
0.4..........0.4...............0.4
=> VCO2=0.6*22.4=13.44 lít
TN3: Giả sử HCO3 phản ứng trước
HCO3- + H+ ------> CO2↑+ H2O
0.5.........0.5...............0.5
CO32- + 2H+ -------> CO2↑+ H2O
0.15.......0.3...................0.15
=> VCO2=0.65*22.4=14.56 lít
Giả sử CO32- phản ứng trước
CO32-+ 2H+ --------> CO2↑+ H2O
0.2........0.4..................0.2
HCO3-+ H+ ---------> CO2↑+ H2O
0.4.........0.4..................0.4
=> VCO2=0.6*22.4=13.44 lít
Do đó thể tích CO2 nằm trong khoảng: 13.44<VCO2<14.56
Bài 6
nH2=0.7 mol
Ta luôn có nSO42-=nH2SO4=nH2=0.7 mol
=> x=mmuối-mgốc axit=82.9-96*0.7=15.7 g