Để điều chế khí oxi từ KClO3 có thể dùng dụng cụ nào sau đây
Ống nghiệm
Bình kíp
Ống sinh hàn
Bình cầu có nhánh
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Sai. Vì CaCO3 → CaO + CO2
b) Đúng. Vì oxi nặng hơn không khí nên được dùng phương pháp đẩy không khí để ngửa bình
c) Sai
d) Đúng. Dùng bông ở ống nghiệm chứa X
e) Đúng.

Tham khảo:
Mục đích của các thao tác thực nghiệm (ghi chữ đậm) trong quy trình: Khuấy và đun sôi: để toluene dễ phản ứng với KMnO4 vì phản ứng này xảy ra ở điều kiện có nhiệt độ.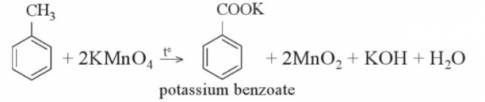
- Lọc bỏ chất rắn kết tinh, cô đặc: Sau phản ứng, trong sản phẩm có MnO2 là chất rắn cần lọc bỏ, cô đặc phần dung dịch lọc có thu được C6H5COOK.
- Acid hoá: acid hóa C6H5COOK bằng HCl để có benzoic acid.
C6H5COOK + HCl → C6H5COOH + KCl
- Lọc lấy chất rắn, kết tinh lại: MnO2 tạo thành thường hấp thụ một lượng lớn sản phẩm. Do đó ta cần rửa lại MnO2 với nước để có sản phẩm sạch.
nC6H5COOH = \(\dfrac{5000}{160}\) = 31,25 mol
C6H5CH3 + 2KMnO4 → C6H5COOK + 2MnO2 + KOH + H2O
31,25 mol 31,25 mol
C6H5COOK + HCl → C6H5COOH + KCl
31,25 mol 31,25 mol
Theo lí thuyết, khối lượng toluene cần để điều chế là: mLT = 31,25.92 = 2875 g. Theo thực tế, hiệu suất của quá trình tổng hợp là 80% thì cần số kg toluene là: mTT =\(\dfrac{2875}{0.8}\) = 3594 g = 3,594 kg.

Đáp án D
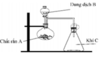
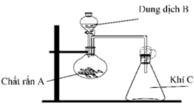
Dung dịch B là dung dịch HCl, chất rắn A là CaCO3
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Chú ý: Theo hình vẽ khi thu như vậy phải có đặc điểm nặng hơn không khí thì chỉ có NO và CO2 là thỏa mãn, tuy nhiên NO tạo ra nó sẽ hóa nâu ngay chuyển hóa thành NO2 nên không thỏa mãn.
3Cu + 8HNO3 loãng → 3Cu(NO3)2 +2NO + 4H2O
2NO + O2 → 2NO2

Đáp án D
Khi thu khí để ngửa bình chứa ⇒ Khí đó nặng hơn không khí.
Mà CO2 có M = 44 > 29 (Không khí).
⇒ Có thể dùng bộ dụng cụ trên để điều chế khí CO2

Câu trả lời đúng là C.
PT: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Từ phản ứng này ⇒ có thể điều chế khí H2
Khí H2 nhẹ hơn không khí nên úp ngược ống nghiệm sẽ thu được khí H2

K M n O 4 K C l O 3 , H 2 O , H 2 O và ít tan trong nước, úp ngược miệng ống nghiệm vào trong nước.

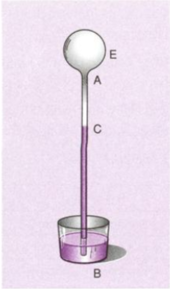
+ Khi thời tiết nóng lên, không khí trong bình cầu cũng nóng lên, nở ra đẩy mực nước trong ống thuỷ tinh xuống dưới.
+ Khi thời tiết lạnh đi, không khí trong bình cầu cũng lạnh đi, co lại dẫn đến mức nước trong ống thuỷ tinh khi đó dâng lên.
Như vậy nếu gắn vào ống thuỷ tinh một băng giấy có chia vạch, thì có thể biết được lúc nào mức nước hạ xuống, dâng lên, tức là khi nào trời nóng, trời lạnh.

Khi thời tiết nóng lên, không khí trong bình cầu cũng nóng lên, nở ra đẩy mực nước trong ống thuỷ tinh xuống dưới. Khi thời tiết lạnh đi, không khí trong bình cầu cũng lạnh đi, co lại dẫn đến mức nước trong ống thuỷ tinh khi đó dâng lên. Nếu gắn vào ống thuỷ tinh một băng giấy có chia vạch, thì có thể biết được lúc nào mức nước hạ xuống, dâng lên, tức là khi nào trời nóng, trời lạnh
- Khi thời tiết nóng lên, không khí trong bình cầu cũng nóng lên, nở ra đẩy mực nước trong ống thủy tinh xuống dưới.
- Khi thời tiết lạnh đi, không khí trong bình cầu cũng lạnh đi, co lại đẩy mực nước trong ống thủy tinh lên trên.

Theo định luật bảo toàn khối lượng, ta có khối lượng khí oxi thu được là:
m O 2 = 24,5 – 13,45 = 11,05(g)
Khối lượng thực tế oxi thu được: m O 2 = (11,05 x 80)/100 = 8,84 (g)

ống nghiệm