Viết Phương Trình Hóa Học của O2 với lần lượt các chất:
Al,Fe,C,S,P
Bt sản phẩm là Al2O3,Fe3O4,CO2,SO2,P2O5
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(S+O_2\rightarrow\left(t^o\right)SO_2\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
Đọc tên sản phẩm:
SO2 : Lưu huỳnh dioxit
Al2O3: Nhôm oxit
MgO: Magie oxit

\(C+O_2\underrightarrow{t^0}CO_2\) ( Cacbon dioxit)
\(4P+5O_2\underrightarrow{t^0}2P_2O_5\)( Diphotpho pentaoxit)
\(H_2+\dfrac{1}{2}O_2\underrightarrow{t^0}H_2O\) ( Nước hay dihidro monooxit)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\) ( Nhôm oxit)

C + O2 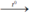 CO2. Cacbon đioxit.
CO2. Cacbon đioxit.
4P + 5O2 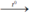 2P2O5. Điphotpho pentaoxit.
2P2O5. Điphotpho pentaoxit.
2H2 + O2 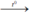 2H2O. Nước.
2H2O. Nước.
4Al + 3O2 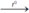 2Al2O3. Nhôm oxit.
2Al2O3. Nhôm oxit.

Bài 8:
\(V_{O_2}=20.100=2000\left(ml\right)=2\left(l\right)\\ a,PTHH:2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ n_{O_2}=\dfrac{2}{22,4}=\dfrac{5}{56}\left(mol\right)\\ n_{O_2\left(p.ứ\right)}=\dfrac{5}{56}.90\%=\dfrac{9}{112}\left(mol\right)\\ n_{KMnO_4\left(dùng\right)}=\dfrac{9}{112}.2=\dfrac{9}{56}\left(mol\right)\\ \Rightarrow m_{KMnO_4}=\dfrac{9}{56}.158=\dfrac{711}{28}\left(g\right)\\ b,2KClO_3\rightarrow\left(t^o,xt\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{56}.\dfrac{2}{3}=\dfrac{1}{42}\left(mol\right)\\ m_{KClO_3}=122,5.\dfrac{1}{42}=\dfrac{35}{12}\left(g\right)\)
Bài 1:
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
Tên sản phẩm: Cacbon dioxit/ Khí cacbonic
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
Tên sản phẩm: Điphotpho pentaoxit
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
Tên sản phẩm: Nước
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Tên sản phẩm: Nhôm oxit

2Mg + O2 ---to --> 2MgO
2H2 + O2 ---to ---> 2H2 O
4Al + 3O2 --to --> 2Al2O3
3Fe + 2O2 --to --> Fe3O4

4P+5O2➞(to)2P2O5
2Cu+O2➞(to)2CuO
3Fe+2O2➞(to)Fe3O4
P2O5:điphotphopentaoxit
CuO:đồng(II)oxit
Fe3O4:oxit sắt từ
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\\ 2Cu+O_2\underrightarrow{t^o}2CuO\\ 3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)

a) $4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
b) $Mg + Cl_2 \xrightarrow{t^o} MgCl_2$
c) $2Na + 2H_2O \to 2NaOH + H_2$
d) $C + O_2 \xrightarrow{t^o} CO_2$
e) $C_xH_y + (x + \dfrac{y}{4})O_2 \xrightarrow{t^o} xCO_2 + \dfrac{y}{2}H_2O$
f) $2Al + Fe_2O_3 \xrightarrow{t^o} Al_2O_3 + 2Fe$
g) $2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
i) $Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2$
k) $Fe_2O_3 + 6HCl \to 2FeCl_3 +3 H_2O$
l) $3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$

1. Pư hóa hợp
\(4K+O_2\underrightarrow{t^o}2K_2O\)
\(4Na+O_2\underrightarrow{t^o}2Na_2O\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
2. Pư hóa hợp
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
3. Pư hóa hợp
\(Na_2O+H_2O\rightarrow2NaOH\)
\(K_2O+H_2O\rightarrow2KOH\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
4. Pư hóa hợp
\(CO_2+H_2O⇌H_2CO_3\)
\(SO_2+H_2O⇌H_2SO_3\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
5. Pư phân hủy.
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
6. Pư thế
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
7. Pư thế
\(2K+2HCl\rightarrow2KCl+H_2\)
\(2K+H_2SO_4\rightarrow K_2SO_4+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
1, 4Al + 3O2 → 2Al2O3
2, 3Fe + 2O2 → Fe3O4
3, C + O2 → CO2
4, S + O2 → SO2
5, 4P + 5O2 → 2P2O5
1. 4Al+3O2---->2Al2O3
2. 3Fe+2O2------>Fe3O4
3. C+O2------>CO2
4. S+O2----->SO2
5. 4P+5O2----->2P2O5
Học tốt ^^