tính lượng quặng sắt có chứa 69.6% fe3o4 để điều chế 12.6 tấn sắt
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


12.6 tấn sắt = 12600 kg
MFe3O4 = 56*3 + 16*4= 232 (g/mol)
Trong 232 g Fe3O4 có 168 g Fe
x g Fe3O4 (= 12600 g Fe
mFe304 = x = 12600*232 : 168 = 17400 (kg)
KL quặng sắt chứa 69,6% Fe304 là
17400 * 100 : 69.6 = 25000 (kg)

1 tấn=100000kg
\(m_{Fe_3O_4}=1000000.90\%=900000\left(g\right)\)
\(\rightarrow n_{Fe_3O_4}=\dfrac{900000}{232}=\dfrac{112500}{29}\left(mol\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(\dfrac{112500}{29}\) \(\dfrac{337500}{87}\) (mol)
\(\rightarrow m_{Fe}=\dfrac{337500}{87}.56\approx217241,38\left(g\right)\approx217,24\left(kg\right)\)
b.
\(n_{Fe}=\dfrac{1000000}{56}=\dfrac{125000}{7}\left(mol\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(\dfrac{375000}{7}\) \(\dfrac{125000}{7}\) (mol)
\(\rightarrow m_q=\dfrac{375000}{7}.232.100:90=13809523\left(g\right)=13809,5\left(kg\right)\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\)

a) PTHH:
Fe3O4 + 4CO =(nhiệt)=> 3Fe + 4CO2
1 (mol)------------------------3 (mol)
232(kg)----------------------168(kg)
900 (kg)----------------------x (kg)
Ta có: Khối lượng Fe3O4 có trong 1 tân quặng là: mFe3O4 = 1 x 90% = 0.9 (tấn ) = 900 (kg)
Lập các tỉ lệ số mol và khối lượng theo phương trình ( x là khối lượng kim loại sắt thu được )
=> x = \(\frac{900\times168}{232}\approx651,72\left(kg\right)\)
b)PTHH:
Fe3O4 + 4CO =(nhiệt)=> 3Fe + 4CO2
1 (mol)----------------------3(mol)
232 (tấn)---------------------168 (tấn)
y (tấn)--------------------------1 (tấn)
Lập các số mol và khối lượng trên phương trình ( y là khối lượng Fe3O4 cần dùng )
=> y = \(\frac{1\times232}{168}=1,4\left(t\text{ấn}\right)\)
=> Khối lượng quặng cần dùng: mquặng = \(1,4\div\frac{90}{100}=1,556\left(t\text{ấn}\right)\)

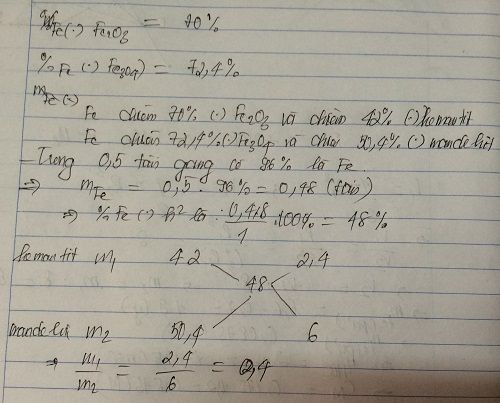
đề sai sai nha !
X là quặng hematit chứa 60% Fe2O3, Y là quặng manhetit chứa 69,6% Fe3O4. Cần trộn X, Y theo tỉ lệ khối lượng như thế nào để được quặng Z mà từ 1 tấn quặng Z có thể điều chế được 0,5 tấn gang chứa 96% sắt?OK!

Khối lượng Fe có trong quặng: 1x64,15/100 = 0,6415 tấn
Khối lượng Fe có trong gang: 0,6415 x (100-2)/100 = 0,62867 tấn
Khối lượng gang sản xuất được: 0,62867 x 100/95 ≈ 0,662 tấn

Gọi khối lượng quặng chứa 75% sắt đem trộn là x tấn,
Gọi khối lượng quặng chứa 50% sắt đem trộn là y tấn (x, y > 0)
Theo đề bài ta có hệ phương trình:
x + y = 25 75 % x + 50 % y = 66 % .25 ⇔ x + y = 25 0 , 75 x + 0 , 5 y = 16 , 5 ⇔ 0 , 5 x + 0 , 5 y = 12 , 5 0 , 75 x + 0 , 5 y = 16 , 5 ⇔ 0 , 25 x = 4 x + y = 25 ⇔ x = 16 y = 9 ( t m d k )
Vậy khối lượng quặng chứa 75% sắt đem trộn là 16 tấn
Đáp án:A
12.6 tấn sắt = 12600 kg
MFe3O4 = 56*3 + 16*4= 232 (g/mol)
Trong 232 g Fe3O4 có 168 g Fe
x g Fe3O4 (= 12600 g Fe
mFe304 = x = 12600*232 : 168 = 17400 (kg)
KL quặng sắt chứa 69,6% Fe304 là
17400 * 100 : 69.6 = 25000 (kg)
tham khảo nhécòn 1 bài mk vừa gửi đó