Tình hóa trị của nguyên tố sau: CuO HF SO3 k20 K2S Co2 Phân loại các hợp chất trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


-
K
2
S
: Ta có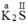
Theo quy tắc hóa trị: a.2 = II.1 → a = 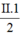 = I
= I
Vậy K có hóa trị I.
- MgS: Ta có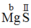
Theo quy tắc hóa trị: b.1 = II.1 → b = 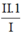 = II
= II
Vậy Mg có hóa trị II.
-
C
r
2
S
3
: Ta có 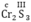
Theo quy tắc hóa trị: c.2 = II.3 → c = 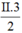 = III
= III
Vậy Cr có hóa trị III.
-
C
S
2
: Ta có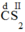
Theo quy tắc hóa trị: d.1 = II.2 → d = 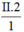 = IV
= IV
Vậy C có hóa trị IV.

a) Fe hóa trị III
b) Cu hóa trị III
c) Cu hóa trị II
d) Ba hóa trị II

| CTHH | Phân loại | Gọi tên |
| P2O3 | oxit axit | điphotpho trioxit |
| FeO | oxit bazơ | sắt (II) oxit |
| CO2 | oxit axit | cacbon đioxit |
| CuO | oxit bazơ | đồng (II) oxit |
| Fe2O3 | oxit bazơ | sắt (III) oxit |
| SO3 | oxit axit | lưu huỳnh trioxit |
| N2O5 | oxit axit | đinitơ pentaoxit |
| Na2O | oxit bazơ | natri oxit |
| P2O5 | oxit axit | điphotpho pentaoxit |
| HgO | oxit bazơ | thuỷ ngân (II) oxit |
| SO2 | oxit axit | lưu huỳnh đioxit |
| Ag2O | oxit bazơ | bạc oxit |
| K2O | oxit axit | kali oxit |

- K2O : Kali oxit
- Al2O3 : Nhôm oxit
- N2O5 : dinito pentaoxit
- SO3 : lưu huỳnh trioxit
- ZnO : Kẽm oxit
- CuO : Đồng (II) oxit
- Fe2O3 : Sắt (III) oxit
- P2O5 : diphotpho pentaoxit
- CaO : Canxi oxit
- SO2 : lưu huỳnh dioxit
K20; oxit bazo : kali oxit
Al2O3; oxit bazo : nhôm oxit
N2O5; oxit axit : đinitopentaoxit
SO3; oxit axit : lưu huỳnh trioxit
ZnO;oxit bazo: kẽm oxit
CuO;oxit bazo: đồng 2 oxit
Fe2O3; oxit bazo : sắt 3 oxit
P2O5;oxit axit : điphotphopentaoxit
CaO;oxit bazo: canxi oxit
SO2 oxit axit : lưu huỳnh đioxit

Câu I:
H(I) và Br(I), H(I) và S(II), N(III) và H(I), Si(IV) và H(I), H(I) và SO4 (II), H(I) và PO4(III), H(I) và NO3(I), Na(I) và O(II), Ba(II) và O(II), Al(III) và O(II), C(IV) và O(II), S(VI) và O(II), P(V) và O(II)

O có số oxi hóa -2, H có số oxi hóa + 1
⇒ Số oxi hóa của các nguyên tố trong các phân tử và ion là:
CO2: x + 2.(-2) = 0 ⇒ x = 4 ⇒ C có số oxi hóa +4 trong CO2
H2O: H có số oxi hóa +1, O có số oxi hóa -2.
SO3: x + 3.(-2) = 0 ⇒ x = 6 ⇒ S có số oxi hóa +6 trong SO3
NH3: x + 3.1 = 0 ⇒ x = -3 ⇒ N có số oxi hóa -3 trong NH3
NO: x + 1.(-2) = 0 ⇒ x = 2 ⇒ N có số oxi hóa +2 trong NO
NO2: x + 2.(-2) = 0 ⇒ x = 4 ⇒ N có số oxi hóa +4 trong NO2
Cu2+ có số oxi hóa là +2.
Na+ có số oxi hóa là +1.
Fe2+ có số oxi hóa là +2.
Fe3+ có số oxi hóa là +3.
Al3+ có số oxi hóa là +3.
NH4+ có số õi hóa là -3

| CTHH | Phân loại | Gọi tên |
| K2S | Muối | Kali sunfua |
| H2SO4 | Axit | Axit sunfuric |
| Pb(OH)2 | Bazo | Chì (II) hidroxit |
| SO3 | Oxit | Lưu huỳnh trioxit |
Quy ước: H(I), O(II)
CuO - Oxit
\(Đặt:Cu^aO^{II}\left(a:nguyên,dương\right)\\ \Rightarrow1.a=1.II\\ \Leftrightarrow a=\dfrac{1.II}{1}=II\\ \Rightarrow Cu\left(II\right)\)
HF - Axit
\(Đặt:H^IF^b\left(b:nguyên,dương\right)\\ \Rightarrow I.1=b.1\\ \Leftrightarrow b=\dfrac{I.1}{1}=I\\ \Rightarrow F\left(I\right)\)
SO3 - Oxit
\(Đặt:S^aO_3^{II}\left(a:nguyên,dương\right)\\ \Rightarrow a.1=II.3\\ \Leftrightarrow a=\dfrac{II.3}{1}=VI\\ \Rightarrow S\left(VI\right)\)
K2O - Oxit
\(Đặt:K_2^aO^{II}\left(a:nguyên,dương\right)\\ \Rightarrow a.2=II.1\\ \Leftrightarrow a=\dfrac{II.1}{2}=I\\ \Rightarrow K\left(I\right)\)
K2S - Muối
\(Đặt:K^a_2S^b\left(a,b:nguyên,dương\right)\\ \Rightarrow2.a=1.b\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{1}{2}=\dfrac{I}{II}\\ \Rightarrow\left\{{}\begin{matrix}a=I\\b=II\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}K\left(I\right)\\S\left(II\right)\end{matrix}\right.\)
CO2 - Oxit.
\(Đặt:C^aO^{II}_2\left(a:nguyên,dương\right)\\ \Rightarrow a.1=II.2\\ \Leftrightarrow a=\dfrac{II.2}{1}=IV\\ \Rightarrow C\left(IV\right)\)