bài 1 : cho 100ml dd H3PO4 1M tác dụng với 200g dd KOH 9,8% thu được dd X. cô cạn dd X thu được m gam chất rắn khan. xác định m
bài 2 : hòa tan 14,2g P2O5 vào 200ml dd NaOH 1M (có D =1,12g/ml) thu được dung dịch X. tính nồng đô phần trăm của dung dịch X.
giúp em với ạ, em cảm ơn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Ta có: nAxit glutamic = 0,09 mol, nHCl = 0,2 mol
⇒ ∑nCOOH + H+ = 0,09×2 + 0,2 = 0,38 mol.
+ nNaOH = 0,34 mol < ∑nCOOH + H+ = 0,38 mol ⇒ nH2O tạo thành = 0,38 mol.
Bảo toàn khối lượng ta có:
mChất rắn = 13,23 + 0,2×36,5 + 0,4×40 – 0,38×18 = 29,69 gam

\(n_{HCl}=2.0,2=0,4\left(mol\right)\) ; \(n_{NaOH}=\dfrac{8\%.100}{100\%.40}=0,2\left(mol\right)\)
Pt : \(HCl+NaOH\rightarrow NaCl+H_2O\)
a) Xét tỉ lệ : \(0,4>0,2\Rightarrow HCldư\)
Dung dịch X gồm : NaCl , HCl dư
Cho quỳ tím vào X --> Quỳ tím hóa đỏ (do HCl có tính axit)
b) \(n_{NaOH\left(pư\right)}=n_{NaCl}=0,2\left(mol\right)\)
\(m_{Rắn.khan}=m_{NaCl}=0,2.58,5=11,7\left(g\right)\)

nKOH : nNaOH = 1,25 : 0,75 = 5 : 3
=> Gộp 2 kiềm thành ROH (2V mol) với R = \(\dfrac{39,5+23,3}{8}\) = 33
nP2O5 = 0,05 =>; nH3PO4 = 0,1
+ Nếu sản phẩm là RH2PO4 (0,1 mol)
=> mRH2PO4 = 13
Nếu sản phẩm là R2HPO4 (0,1 mol)
=> mR2HPO4 = 16,2
+ Nếu sản phẩm là R3PO4 (0,1 mol)
=>mR3PO4 = 19,4
Theo đề thì m rắn = 24,4 > 19,4
=>Chất rắn gồm R3PO4 (0,1 mol) và ROH dư
->nROH dư = 0,1
Bảo toàn R
->nROH = 2V = 0,4
=>V = 0,2 lít = 200 ml.

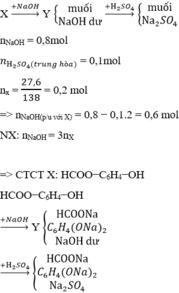
nNaOH = 0,2mol
n H 2 S O 4 ( t r u n g h ò a ) = 0,02mol
nx = 9,12/152 = 0,06 mol => nNaOH(p/u với X) = 0,2 − 0,01.2 = 0,18 mol
−NX: nNaOH = 3nX
=> CTCTX: RCOO−C6H4(R′)−OH
Với R +R' = CH3
RCOO−C6H4(R′)−OH  RCOONa + C6H4(R′)(ONa)2 + 2H2O
RCOONa + C6H4(R′)(ONa)2 + 2H2O
2NaOH +H2SO4 → Na2SO4 + 2H2O
=> nH2O = 2nX + 2 nNaOH dư = 2. 0,06 + 0,01.2 =0,14
Bảo toàn khối lượng cho cả 2 quá trình:
mX + mNaOH + mH2SO4 = mrắn + mH2O
=> mrắn = 15,58 gam
Đáp án cần chọn là: C

Đáp án B
Áp dụng định luật bảo toàn khối lượng có
mX + mddNa/KOH = m chất rắn + mH2O sản phẩm
⇒ mH2O sản phẩm = 16,4 + 0,2. ( 40 + 56) – 31,1 = 4,5
⇒ nH2O sản phẩm = 0,25 < nNaOH + nKOH
⇒ nAxit = nH2O sản phẩm = 0,25 ( dựa vào đáp án thì các Axit đều đơn chức)
⇒ MX = 16,4 : 0,25 = 65,6
Mà 2 Axit đồng đẳng kế tiếp ⇒ 2Axit đó là C2H4O2 và C3H6O2.
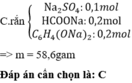
Bài 1: PTHH: \(H_3PO_4+3KOH->K_3PO_4+3H_2O\) Số mol H3PO4: \(n_{H_3PO_4}=1.0,1=0,1\left(mol\right)\) Khối lượng KOH: \(m_{KOH}=\dfrac{9,8.200}{100}=19,6\left(g\right)\) Số mol KOH: \(n_{KOH}=\dfrac{19,6}{56}=0,35\left(mol\right)\) Lập tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,35}{3}\) => KOH dư, tính toán theo H3PO4. Theo PTHH, ta có: \(n_{K_3PO_4}=n_{H_3PO_4}=0,1\left(mol\right)\) Khối lượng K3PO4 cần tìm: \(m_{K_3PO_4}=0,1.212=21,2\left(g\right)\) Bài 2: PTHH: \(P_2O_5+6NaOH->2Na_3PO_4+3H_2O\) Số mol P2O5: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\) Số mol NaOH: \(n_{NaOH}=1.0,2=0,2\left(mol\right)\) Lập tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,2}{6}\) => P2O5 dư, tính toán theo NaOH. Theo PTHH, ta có: \(n_{Na_3PO_4}=\dfrac{1}{3}n_{NaOH}=\dfrac{1}{3}.0,2=0,067\left(mol\right)\) Khối lượng Na3PO4: \(m_{Na_3PO_4}=0,067.164=10,988\left(g\right)\) Khối lượng dd NaOH cho phản ứng: \(m_{NaOH}=1,12.200=224\left(g\right)\) Nồng độ % dd X: \(C\%_{Na_3PO_4}=\dfrac{10,988.100\%}{14,2+224}=4,61\%\)