Một dung dịch H2SO4 có nồng độ 14%. Tính khối lượng H2SO4 có trong 150g dung dung dịch?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


bài này không cho CTHH của 2 loại muối thì gần như impossible ;-;

\(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\\ a,CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ b,n_{H_2SO_4}=n_{CuSO_4}=n_{CuO}=0,1\left(mol\right)\\ C_{MddH_2SO_4}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
c, Cần có thêm KLR của dung dịch axit mới tính được em ha

\(C_{MddH_2SO_4}=\dfrac{C\%_{ddH_2SO_4}.10.D_{ddH_2SO_4}}{M_{H_2SO_4}}\\ \Leftrightarrow3,3=\dfrac{C\%_{ddH_2SO_4}.10.1,195}{98}\\ \Leftrightarrow C\%_{ddH_2SO_4}\approx27,063\%\)

Đáp án A
Gọi a là số mol Cu(NO3)2 trước khi điện phân:
Phương trinh phản ứng:
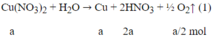
Khi khí bắt đầu thoát ra ở catot (H2 thoát ra do điện phân nước) nghĩa là Cu đã được giải phóng hoàn toàn ở catot. Sau khi để yên dung dịch, sẽ xảy ra phản ứng sau đây:
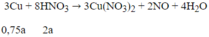
Số mol Cu dư sau phản ứng (2) là 0,25a
Ta có: 0,25a = 3,2/64 → a = 0,2 (mol)
⇒ Nồng độ của Cu(NO3)2 ban đầu là 1M

Đáp án B
Các phản ứng xảy ra:
NH4+ + OH- → NH3↑ + H2O
Mg2+ + 2OH- → Mg(OH)2↓ tủa trắng
Fe3+ + 3OH- → Fe(OH)3↓ nâu đỏ
Al3+ + 3OH- → Al(OH)3↓
Al(OH)3 + 3OH- → [Al(OH)4]- tan
Nhận biết được 4 dung dịch.
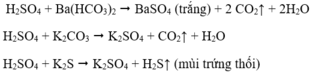
\(m_{H_2SO_4}=\dfrac{14.150}{100}=21\left(g\right)\)