Cho một dòng khí H2 dư qua 4,8 gam hỗn hợp CuO và một oxit sắt nung nóng thu được 3,52 gam chất rắn.Nếu cho chất rắn đó hoà tan trong axit HCl thì thu được 0,896 lít H2 (đktc).Xác định khối lượng mỗi oxit trong hỗn hợp và xác định công thức của oxit sắt.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\) (1)
\(Fe_xO_y+yH_2\xrightarrow[t^o]{}xFe+yH_2O\) (2)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (3)
a) Ta có: \(n_{H_2\left(3\right)}=\dfrac{0,896}{22,4}=0,04\left(mol\right)=n_{Fe}\) \(\Rightarrow n_{Cu}=\dfrac{3,52-0,04\cdot56}{64}=0,02\left(mol\right)=n_{CuO}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CuO}=0,02\cdot80=1,6\left(g\right)\\m_{Fe_xO_y}=4,8-1,6=3,2\left(g\right)\end{matrix}\right.\)
b) Theo PTHH: \(n_{Fe_xO_y}=\dfrac{0,04}{x}=\dfrac{3,2}{56x+16y}\)
\(\Rightarrow0,96x=0,64y\) \(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy CTPT cần tìm là Fe2O3
PTHH: CuO+H2to→Cu+H2OCuO+H2→toCu+H2O (1)
FexOy+yH2→toxFe+yH2OFexOy+yH2→toxFe+yH2O (2)
Fe+2HCl→FeCl2+H2↑Fe+2HCl→FeCl2+H2↑ (3)
a) Ta có: nH2(3)=0,89622,4=0,04(mol)=nFenH2(3)=0,89622,4=0,04(mol)=nFe ⇒nCu=3,52−0,04⋅5664=0,02(mol)=nCuO⇒nCu=3,52−0,04⋅5664=0,02(mol)=nCuO
⇒{mCuO=0,02⋅80=1,6(g)mFexOy=4,8−1,6=3,2(g)⇒{mCuO=0,02⋅80=1,6(g)mFexOy=4,8−1,6=3,2(g)
b) Theo PTHH: nFexOy=0,04x=3,256x+16ynFexOy=0,04x=3,256x+16y
⇒0,96x=0,64y⇒0,96x=0,64y ⇒xy=23⇒xy=23
Vậy CTPT cần tìm là Fe2O3

1 ) CAO +H2O => CA(OH)2 (1)
2K + 2H2O => 2KOH + H2(2)
n (H2) =1,12/22,4 =0,05
theo ptpư 2 : n(K) = 2n (h2) =2.0.05=0,1(mol)
=> m (K) =39.0,1=3,9 (g)
% K= 3,9/9,5 .100% =41,05%
%ca =100%-41,05%=58,95%
xo + 2hcl =>xcl2 +h2o
10,4/X+16 15,9/x+71
=> giải ra tìm đc X bằng bao nhiêu thì ra

a)
Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_xO_y}=b\left(mol\right)\end{matrix}\right.\)
=> 80a + b(56x + 16y) = 4,8 (1)
PTHH: CuO + H2 --to--> Cu + H2O
a------------->a
FexOy + yH2 --to--> xFe + yH2O
b----------------->bx
=> 64a + 56bx = 3,52 (2)
PTHH: Fe + 2HCl --> FeCl2 + H2
bx-------------------->bx
=> \(bx=\dfrac{0,892}{22,4}\approx0,04\left(mol\right)\)
(2) => a = 0,02 (mol)
(1) => by = 0,06
Xét \(\dfrac{bx}{by}=\dfrac{x}{y}=\dfrac{0,04}{0,06}=\dfrac{2}{3}\)
=> CTPT: Fe2O3
=> b = 0,02 (mol)
\(\left\{{}\begin{matrix}m_{CuO}=0,02.80=1,6\left(g\right)\\m_{Fe_2O_3}=0,02.160=3,2\left(g\right)\end{matrix}\right.\)
b) CTPT: Fe2O3

X gồm Fe và Cu. Với HCl:
nFe = nH2 = 0,04
=>nCu = (mX – mFe)/64 = 0,02
=> nCuO = nFexOy = 0,02
-> x = nFe/nFexOy = 2
; Oxit là Fe2O3.
Bảo toàn O: \(m_{O\left(oxit\right)}=m_{giảm}=4,8-3,52=1,28\left(g\right)\)
\(n_{O\left(oxit\right)}=\dfrac{1,28}{16}=0,08\left(mol\right)\\ n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,04 <------------------------ 0,02
\(m_{Cu}=3,52-0,04.56=1,28\left(g\right)\\ n_{O\left(CuO\right)}=n_{Cu}=\dfrac{1,28}{64}=0,02\left(mol\right)\\ n_{O\left(Fe_xO_y\right)}=0,08-0,02=0,06\left(mol\right)\)
CTHH: FexOy
=> x : y = 0,04 : 0,06 = 2 : 3
CTHH Fe2O3

nH2= 0,448/22,4= 0,02(mol)
PTHH :
CuO + H2 -tdo--> Cu + H20
FexOy + yH2 -tdo-> xFe + yH20
Cu + HCl --> k pu
Fe + 2HCl ---> FeCl2 + H2
0,02 -- 0,04---> 0,02 --- 0,02 (mol)
mFe = 0,02 .56= 1,12(g)
=> mCu = 1,76 - 1,12= 0,64(g)
n Cu = 0,64 /64 =0,01(mol)
PTHH :
CuO + H2 -tdo-> Cu + H20
0,,01 --0,01 ----> 0,01(mol)
mCuO= 0,01 . 80 = 0,8(g)
=> mFexOy = 2,4-0,8= 1,6(g)
PTHH :
FexOy + yH2 ---> xFe + yH20
56x+ 16y ---------> 56x
1,6 (g) -------------> 1,12(g)
<=> 1,6 .56x = 1,12( 56x + 16y)
<=> 89,6x = 62,72 x + 17,92y
<=> 89,6x - 62,72x = 17,92y
<=> 26,88 x = 17,92y
=> x/y= 17,92 / 26,88 =2/3
Vậy công thức đúng là Fe203.

a, \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,04<-----------------------0,04
\(m_{Cu}=3,52-0,04.56=1,28\left(g\right)\)
Bảo toàn O: \(\left\{{}\begin{matrix}n_{O\left(oxit\right)}=\dfrac{4,8-3,52}{16}=0,08\left(mol\right)\\n_{O\left(CuO\right)}=n_{Cu}=\dfrac{1,28}{64}=0,02\left(mol\right)\end{matrix}\right.\)
=> \(n_{O\left(Fe_xO_y\right)}=0,08-0,02=0,06\left(mol\right)\)
PTHH:CuO + H2 --to--> Cu + H2O
0,02<--------------0,02
=> \(\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{0,02.80}{4,8}.100\%=33,33\%\\\%m_{Fe_xO_y}=100\%-33,33\%=66,67\%\end{matrix}\right.\)
b, CTHH là FexOy
=> x : y = 0,04 : 0,06 = 2 : 3
=> CTHH là Fe2O3
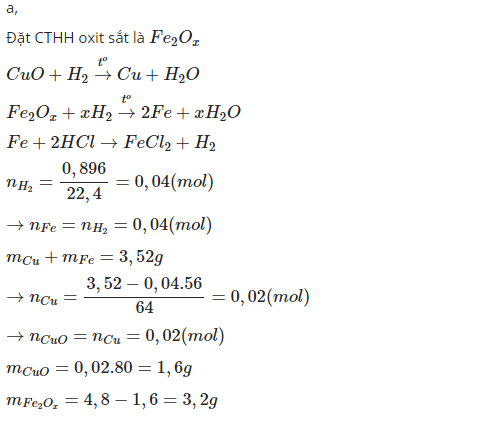
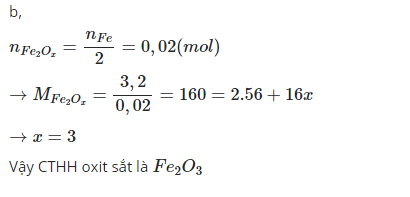
Phương trình phản ứng:
FE+2HCL->Fecl2+H2
Số mol H2 = 0,896/22,4 = 0,04 mol => Mol Fe = 0,04 mol => Số g Cu = 3,52 - 56x0,04 = 1,28
=> Khối lượng CuO trong hỗn hợp ban đầu = (1,28/64)x(64+16) = 1,6g => Số g oxit sắt = 4,8-1,6 = 3,2g.
Gọi công thức của oxit sắt là: FexOy.
Ta có số mol của oxit sắt:32/(56x+16y) = 0,04/x
Giải ra ta được tỉ lệ x/y = 2/3 => Công thức phân tử của oxit sắt là: Fe2O3
Gọi CTHH của oxit sắt là: FexOy
PTHH: CuO + H2 -> Cu + H2O (1)
FexOy + H2 -> xFe + H2O (2)
Fe + HCl -> FeCl2 + H2 (3)
(Chất rắn thu được sau phản ứng là Cu và Fe nhưng Cu ko tác dụng được vs HCl nên chỉ có Fe)
nH2 (ĐKTC) \(\frac{0,896}{22,4}=0,04\left(mol\right)\)
nFe = nH2 = 0,04 mol => mFe = 0,04 . 56 = 2,24 (g)
mCu = 3,52 - 2,24 = 1,28 (g)
mCuO trong hỗn hợp b.đầu: \(\frac{1.28}{64}.80=1,6\left(g\right)\)
mFexOy = 4,8 - 1,6 = 3,2 (g)
nFexOy = \(\frac{3,2}{56x+16y}=\frac{0,04}{x}\)
=> \(\frac{x}{y}=\frac{3}{4}\)
=> CTHH của oxit sắt là: Fe3O4