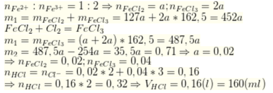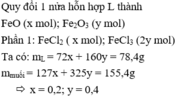Cho m gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 vào một lượng dung dịch HCl 2M vừa đủ, thu được dung dịch Y có tỉ lệ số mol
Fe2+ :Fe3+ =1 : 2. Chia Y thành hai phần bằng nhau. Cô cạn phần 1 thu được m1 gam muối khan. Sục khí clo dư vào phần 2, cô cạn dung dịch sau phản ứng thu được m2 gam muối khan.
Biết m2-m1= 3,55. Thẻ tích dung dịch HCl đã dùng là.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy đổi X thành \(\left\{{}\begin{matrix}FeO:a\left(mol\right)\\Fe_2O_3:b\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{Fe^{2+}}=a\left(mol\right)\\n_{Fe^{3+}}=2b\left(mol\right)\end{matrix}\right.\)
=> \(\dfrac{a}{2b}=\dfrac{1}{2}\) => a = b
Phần 1: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
=> 127.0,5a + 162,5b = m1
=> m1 = 226a (g)
Phần 2: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
PTHH: 2FeCl2 + 3Cl2 --> 2FeCl3
0,5a------------->0,5a
=> 162,5(0,5a + b) = m2
=> m2 = 243,75a (g)
Mà m2 - m1 = 0,71
=> 243,75a - 226a = 0,71
=> a = 0,04 (mol)
Y chứa \(\left\{{}\begin{matrix}FeCl_2:0,04\left(mol\right)\\FeCl_3:0,08\left(mol\right)\end{matrix}\right.\)
Bảo toàn Cl: nHCl = 0,32 (mol)
=> \(V_{dd.HCl}=\dfrac{0,32}{2}=0,16\left(l\right)\)

Cho m gam hỗn hợp X gồm FeO, Fe2O3 , Fe3O4 vào một lượng vừa đủ d
Link tham khảo :

Quy đổi X thành \(\left\{{}\begin{matrix}FeO:a\left(mol\right)\\Fe_2O_3:b\left(mol\right)\end{matrix}\right.\)
Phần 1: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
=> 127.0,5a + 162,5b = 74,15
=> 63,5a + 162,5b = 74,15 (1)
Phần 2: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
PTHH: 2FeCl2 + Cl2 --> 2FeCl3
0,5a------------>0,5a
=> 162,5(0,5a + b) = 81,25
=> 0,5a + b = 0,5 (2)
(1)(2) => a = 0,4 (mol); b = 0,3 (mol)
=> m = 0,4.72 + 0,3.160 = 76,8 (g)

Đáp án : C
Coi mỗi phần hỗn hợp oxit gồm FeO và Fe2O3 với số mol là a và b
=> Muối P1 có a mol FeCl2 và 2b mol FeCl3
=> 72a + 160b = 156,8.0,5 = 78,4 và 127a + 325b = 155,4
=> a = 0,2 ; b = 0,4 mol => nCl- (muối 1) = 2,8 mol
Xét cả quá trình thì : muối phần 2 chính là muối phần 1 có 1 lượng SO42- thay thế cho Cl-
Cứ x mol SO42- thay thế cho 2x mol Cl-
=> mmuối 2 - mmuối 1 = 96x – 35,3.2x = 167,9 – 155,4 => x = 0,5 mol
=> Số mol Cl bị thay thế là 1,0 mol => số mol Cl trong muối 2 = 2,8 – 1,0 = 1,8 mol