Câu 1 Xác định A,B,C hoàn thành và viết phương trình cho sơ đồ phản ứng sau:
FeCl3 ↔ A → C → FeCl3
↓ ↑
B →
Câu 2 : Cho hỗn hợp gồm kim loại R hóa trị II và nhôm tác dụng với dung dịch H2SO4 loãng, dư. Khi phản ứng kết thúc thu được dung dịch gồm 2 muối có tổng khối lượng 46,2g và 8,96 lít khí ở đktc. Xác định kim loại R
Câu 3: Cho 4,64 g hỗn hợp 3 kim loại Cu,Mg,Fe tác dụng với dung dịch HCl dư thu được 0,2g khí H2 và 0,64g chất rắn không tan.
Tính tỉ lệ phần trăm về khối lượng của 3 kim loại trong hỗn hợp trên
Câu 4: Giải thích hiện tượng và nêu tác hại của mưa axit, viets các phương trình hóa học xảy ra.
Câu 5:
a, Khí CO2 có lẫn khí CO và O2. Hãy trình bày phương pháp để thu được khí CO2 tinh khiết.
b, Có hỗn hợp gồm Al2O3, SiO2, Fe2O3. Bằng phương pháp hóa học hãy tách riêng từng oxit ra khỏi hỗn hợp
Câu 6:
Không dùng thêm hóa chất nào khác hãy nhận biết các dung dịch sau: HCl, NaOH, Ba(OH)2, K2CO3, MgSO4

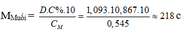
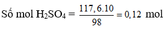
Khi cho hỗn hợp tác dụng với dd ax HCl du có 0,64g chất rắn không tan nên lượng không tan là khối lượng của Cu
\(n_{Cu}=\dfrac{0,64}{64}=0,01\left(mol\right)\\ n_{Mg}=a\left(mol\right)\\ n_{Fe}=b\left(mol\right)\)
Từ đó có \(m_{hh\left(Mg,Fe\right)}=24a+56b=4,64-0,64=4\left(g\right)\left(1\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
theo PTHH có
\(n_{H_2}=a+b=0,1\left(mol\right)\left(2\right)\)
Từ (1) va (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,05\left(mol\right)\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,64\cdot100\%}{4,64}\approx13,793\%\\ \%m_{Mg}=\dfrac{0,05\cdot24\cdot100\%}{4,64}\approx25,862\%\\ \%m_{Fe}=100\%-13,793\%-25,862\%=60,345\%\)
Bước 1: Đốt cháy hỗn hợp khí sẽ có PTHH như sau CO+O2->CO2
Bước 2: Sục hỗn hợp khí sau phản ứng(hỗn hợp khí vì không biết là O2 hết hay CO hết) vào dung dịch nước vôi trong Ca(OH)2 du
PTHH Ca(OH)2+CO2->CaCO3+H2O
Bước 3: Lọc lấy kết tủa và đem đi nung nóng \(CaCO_3\leftrightarrow CaO+CO_2\)
dẫn lượng khí sau phản ứng vào trong một ống nghiệm thế là đã thu được khí CO2 tinh khiết