Câu 1: Cho 0,557 gam (natri) Na tác dụng với H2O dư, thoát ra V lít khí, tính V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\text{Fe+H2SO4=FeSO4+H2}\)
Ta có :
\(\text{nH2=1,792/22,4=0,08mol}\)
\(\text{=>nFe=0,08mol}\)
Khi cho 0,08mol Fe td với HNO3:
Quá trình nhường e: Fe=Fe+3 +3e
=> n e nhường=0,24mol
Theo ĐLBTe, ta có n e cho=n e nhận.
Quá trình nhận e: \(\text{N+5 +3e=>N+2}\)
\(\text{=> nN+2=0,24/3=0,08mol}\)
\(\text{=>nNO=0,08mol =>V NO=0,08.22,4=1,792l}\)
Fe+H2SO4--->FeSO4+H2
Fe+4HNO3---->Fe(NO3)3+NO+2H2O
n H2=0,08(mol)
Theo pthh1
n Fe =n H2 =0,08(mol)
m Fe=0,08.56=4,48(g)=m
Theo pthh2
n NO=n Fe=0,08(mol)
V NO= V=0,08.22,4=1,792(l)

\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\) \(n_{H_2SO_4}=0,3.0,25=0,075\left(mol\right)\)
\(X+H_2SO_{4\left(l\right)}\rightarrow XSO_4+H_2\uparrow\)
0,06 0,06 0,06 0,06 (mol)
dư:0 0,015 0 0 (mol)
b/
m\(M_X=\dfrac{3,36}{0,06}=56\left(g\right)\)
\(\rightarrow Fe\)
c/
\(2Fe+6H_2SO_{4\left(đn\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,06 0,09 (mol)
V\(_{SO_2}=0,09.22,4=2,016\left(l\right)\)

1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl

Tham khảo
Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí
Chất rắn G là Al2O3, MgO, Fe2O3

nMg= 0.84/24=0.035 mol
PTHH: Mg +2HCl ----> MgCl2 + H2
0.035..................................0.035
VH2= 0.035*22.4=0.784 l

\(2C_2H_5OH+2Na\rightarrow2C_2H_5Na+H_2\)
\(2C_3H_7OH+2Na\rightarrow2C_3H_7Na+H_2\)
Ta có:
\(n_{H2}=\frac{4,2}{22,4}=0,1875\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{C2H5OH}:a\left(mol\right)\\n_{C3H7OH}:b\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}0,5a+0,5b=0,1875\\46a+60b=18,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,075\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{C2H5OH}=\frac{0,3.46}{18,3}.100\%=75,41\%\\\%m_{C3H7OH}=100\%-75,41\%=24,59\%\end{matrix}\right.\)

Chia làm hai phần bằng nhau mỗi phần co 8,9g hỗn hợp.
Phần 1:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
x x x
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
y y y
\(\left\{{}\begin{matrix}24x+65y=8,9\\x+y=0,15\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{17}{820}\\y=\dfrac{53}{410}\end{matrix}\right.\)
\(\Rightarrow n_{H_2SO_4}=\dfrac{17}{820}+\dfrac{53}{410}=0,15mol\)
\(a=C_{M_{H_2SO_4}}=\dfrac{0,15}{0,2}=0,75M\)
\(m_{Mg}=2\cdot\dfrac{17}{820}\cdot24=1g\)
\(\Rightarrow m_{Zn}=17,8-1=16,8g\)
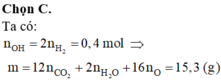

Giải:
Số mol
Phương trình
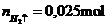

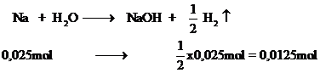
Vậy V=0,28 lit