CẦN GẤP GIÚP EM VỚI Ạ
Cho 0,83 gam hỗn hợp Al và Fe tác dụng với dd H2SO4 loãng, dư. Sau phản ứng thu được 0,56 lít khí ở đktc.
a, Viết PTHH
b, Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.


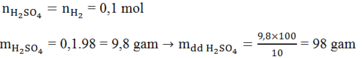
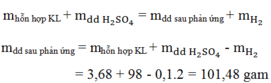

a. 2Al + 3H2SO4 ------> Al2(SO4)3 + 3H2
x 3/2x
Fe + H2SO4 -------> FeSO4 + H2
y y
b. Ta có :
n H2 ( đktc) = 0,56/22,4 = 0,025 mol
Ta có Pt : 27x + 56y = 0,83
3/2x + y = 0,025
=> x = 0.01 mol
y = 0.01 mol
=> m Al = 0,01 . 27 = 0,27g
m Fe = 0,01 . 56 = 0,56g
=> %m Al = 0,27/0,83 .100% = 32,5%
%m Fe = 100% - 32.5% = 67.5%
đặt Al là x theo pt H2 là 3/2X
Fe là y theo pt H2 là y