hòa tan 40g Mgo vào 300g dd H2SO4 98%. Tính nồng độ phần trăm các chất trong dd sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
\(m_{H_2SO_4}=196.40\%=78,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{78,4}{98}=0,8\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Mol: 0,2 0,6 0,2
Ta có: \(\dfrac{0,2}{1}< \dfrac{0,8}{3}\) ⇒ Fe2O3 hết, H2SO4 dư
mdd sau pứ = 32 + 196 = 228 (g)
\(C\%_{ddFe_2\left(SO_4\right)_3}=\dfrac{0,2.400.100\%}{228}=35,09\%\)
\(C\%_{ddH_2SO_4dư}=\dfrac{\left(0,8-0,6\right).98.100\%}{228}=8,596\%\)

Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Ta lại có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{294}.100\%=20\%\)
=> \(m_{H_2SO_4}=58,8\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
Ta thấy: \(\dfrac{0,2}{1}=\dfrac{0,6}{3}\)
Vậy không có chất dư.
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)
Ta có: \(m_{dd_{Al_2\left(SO_4\right)_3}}=294+5,4-\left(\dfrac{3}{2}.0,2.2\right)=298,8\left(g\right)\)
=> \(C_{\%_{Al_2\left(SO_4\right)_3}}=\dfrac{34,2}{298,8}.100\%=11,45\%\)

\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,02 0,02
\(n_{CuSO4}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
⇒ \(m_{CuSO4}=0,02,160=3,2\left(g\right)\)
\(m_{ddspu}=1,6+300=301,6\left(g\right)\)
\(C_{CuSO4}=\dfrac{3,2.100}{301,6}=1,6\)0/0
Chúc bạn học tốt

a) Đặt: nMg=x(mol); nZnO=y(mol)
nH2SO4= 0,2(mol)
PTHH: Mg + H2SO4 -> MgSO4 + H2
x___________x____x_______x(mol)
ZnO + H2SO4 -> ZnSO4 + H2O
y____y______y(mol)
Ta có:
\(\left\{{}\begin{matrix}24x+81y=12,9\\22,4x=4,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
mMg=0,2.24=4,8(g)
%mMg=(4,8/12,9).100=37,209%
=>%mZnO=62,791%
b) nH2SO4=x+y=0,3(mol)
=> \(C\%ddH2SO4=\dfrac{0,3.98}{120}.100=24,5\%\)

\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{200\cdot39.2\%}{98}=0.8\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Lập tỉ lệ :
\(\dfrac{0.2}{2}< \dfrac{0.8}{3}\) => H2SO4 dư
\(n_{H_2}=\dfrac{3}{2}\cdot0.2=0.3\left(mol\right)\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(m_{dd}=5.4+200-0.3\cdot2=204.8\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0.1\cdot342=34.2\left(g\right)\)
\(C\%_{Al_2\left(SO_4\right)_3}=\dfrac{34.2}{204.8}\cdot100\%=16.7\%\)

thôi thì mình làm cho bn vậy, câu a ko làm dc đâu, làm câu b thôi, làm sao biết dc chất nào dư khi chỉ có số mol 1 chất?
nK2SO3=0.1367(mol)
mddH2SO4=Vdd.D=200.1,04=208(g)
K2SO3+H2SO4-->K2SO4+H2O+SO2
0.1367----0.1367----0.1367---------0.1367 (mol)
mddspu=100+208-0,1367.64=299.2512(g) ; mK2SO4=0,1367.174=23.7858(g)
==>C%=23.7858.100/299.512=7.94%
2)pt bn tự ghi nhé
ta có hệ pt: 56a+27b=11 và a+3b/2=8.96/22.4==>a=0.1, b=0.2
==>%Fe=0.1x56x100/11=50.9%
%Al=100%-50.9%=49.1%
b)nH2SO4= 0.7(mol)==>VddH2SO4=0.7/2=0.35(L)

Bài 4 :
\(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
300ml = 0,3l
\(n_{HCl}=1.0,3=0,3\left(mol\right)\)
1) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,1 0,3 0,1
2) Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\)
⇒ MgO phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của MgO
\(n_{MgCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{MgCl2}=0,1.95=9,5\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,3-\left(0,1.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddHCl}=1,14.300=342\left(g\right)\)
\(m_{ddspu}=4+342=346\left(g\right)\)
\(C_{MgCl2}=\dfrac{9,5.100}{346}=2,75\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{3,65.100}{346}=1,05\)0/0
Chúc bạn học tốt

Ta có: \(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
PTHH: MgO + 2HCl ---> MgCl2 + H2.
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,1\left(mol\right)\)
=> \(m_{MgCl_2}=0,1.95=9,5\left(g\right)\)
Ta có: \(m_{dd_{MgCl_2}}=4+100=104\left(g\right)\)
=> \(C_{\%_{MgCl_2}}=\dfrac{9,5}{104}.100\%=9,13\%\)

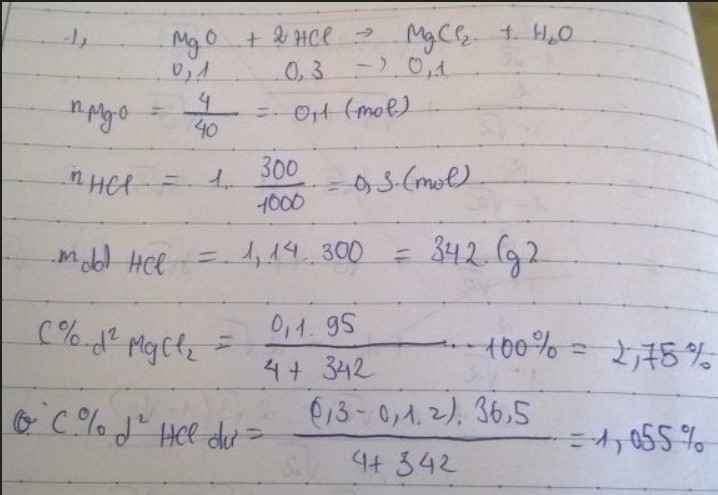
PTHH: \(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{40}{40}=1\left(mol\right)\\n_{H_2SO_4}=\dfrac{300\cdot98\%}{98}=3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{MgSO_4}=1\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{120}{300+40}\cdot100\%\approx35,3\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{2\cdot98}{300+40}\cdot100\%\approx57,65\%\end{matrix}\right.\)