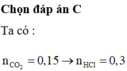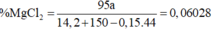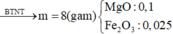hòa tan hết 14,2 g hỗn hợp A gồm MgCO3 và muối cacbonat của kim loại R bằng lượng vừa đủ dung dịch HCl 7,3% thu được dung dịch D và 3,36 l khí CO2 ở đktc . Thêm 32,4 g nước vào dung dịch D được dung dịch E . Nồng độ của MgCl2 trong dung dịch E là 5% . Xác định kim loại R và thành phần % theo khối lượng của mỗi chất trong hỗn hợp A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(MgCO_3\left(a\right)+2HCl\rightarrow MgCl_2\left(a\right)+H_2O+CO_2\left(a\right)\)
\(R_2\left(CO_3\right)_x\left(b\right)+2xHCl\rightarrow2RCl_x+xH_2O+xCO_2\left(bx\right)\)
Gọi a,b lần lượt là số mol của MgCO3, R2(CO3)x trong A(a,b > 0; x là hóa trị của R \(\in N\)*)
\(n_{CO_2}=0,15\left(mol\right)\Rightarrow a+bx=0,15\left(I\right)\)
\(m_{HCl}=0,15.36,5.2=10,95\left(g\right)\)
\(\Rightarrow m_{ddHCl}=10,95.7,3\%=150\left(g\right)\)
\(m_{ddsaupư}=m_A+m_{ddHCl}-m_{CO_2}=14,2+150-0,15.44=157,6\left(g\right)\)
\(\Rightarrow m_{ddE}=32,4+157,6=190\left(g\right)\)
Vì \(\%MgCl_2\left(trongE\right)=5\%\Rightarrow\dfrac{9500a}{190}=5\)
\(\Rightarrow a=0,1\)
Thay vào (I) :
\(\Rightarrow bx=0,15-0,1=0,05\left(II\right)\)
Do mA = 14,2g \(\Rightarrow8,4+b\left(2M_R+60x\right)=14,2\)
\(\Rightarrow2bM_R+60bx=5,8\left(III\right)\)
Thay (II) vào (III) \(\Rightarrow2bM_R=2,8\Rightarrow M_R=28x\)
Kẻ bảng biện luận x = I, II, hoặc III
\(\Rightarrow R\) là Fe (II) .
\(\%m_{MgCO_3}\approx59,15\%\)
\(\%m_{FeCO_3}=40,85\%\)

Mk trình bày lại nhé
Gọi CTHH của muối cacbonat của R là R2(CO3)n ( n là hóa trị của R)
MgCO3 + 2HCl → MgCl2 + CO2↑ + H2O (1)
R2(CO3)n + 2nHCl → 2RCln + nCO2↑ + nH2O (2)
nCO2 =\(\frac{3,36}{22,4}\) = 0,15 mol
nHCl p.ứ = 2nCO2 = 0,3 mol
mHCl = 0,3 . 36,5 = 10,95 (g)
mdd HCl = \(\frac{10,95}{7,3}\). 100 = 150 (g)
mD = mC + mdd HCl - mCO2
= 14,2 + 150 - 0,15 . 44
= 157,6 (g)
mMgCl2 = 157,6 . 6,028% = 9,5 (g)
nMgCl2 = \(\frac{9,5}{95}\) = 0,1 (mol)
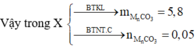
Theo (1): nMgCO3 = nCO2 (1) = nMgCl2 = 0,1 mol
nCO2 (2) = 0,15 - 0,1 = 0,05 mol
Theo (2): nR2(CO3)n =\(\frac{nCO2\left(2\right)}{n}=\frac{0,05}{n}\)
mC = mMgCO3 + mR2(CO3)n
→ 0,1 . 84 +\(\frac{0,05}{n}\)
. (2MR + 60n) = 14,2
→ MR = 28n
→ n = 2; MR = 56
→ R là Sắt
%mMgCO3 = 0,1 . 84 : 14,2 . 100% = 59,15%
%mFeCO3 = 100% - 59,15% = 40,85%

nCO2 = 0,15 mol
MgCO3 + 2HCl ---> MgCl2 + CO2 + H2O
0.1 0,1 --> 0,1
RCO3 + 2HCl ---> RCl2 + CO2 + H2O
0,05 <---- (0,15-0,1)
Ta thấy: n HCl = 2n CO2 = 2.0,15 = 0,3 mol
m dd HCl = (0,3.36,5).100/7,3 = 150g
m CO2 = 0,15.44 = 6,6g
m dd sau phản ứng = m X + m dd HCl - m CO2 = 157,6 g
m MgCl2 = m dd sau phản ứng.C%/100 ~ 9,5g
n MgCl2 = 0,1 mol (thế vào pt trên)
Ta có: m RCO3 = m X - m MgCO3
=> 0,05(R + 60) = 14,2 - 0,1.84
=> R = 56
Vậy R là Fe
Chúc em học tốt!!