hấp thụ toàn bộ m gam hỗn hợp CO2 và hơi nước vào 9000ml dung dịch Ca(OH)2 0,01M thu được 4g kết tủa. Tách bỏ phần kết tủa, thấy khối lượng dung dịch tăng 1,82 gam so với khối lượng dung dịch Ca(OH)2 ban đầu. Tính gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



C2H4, C3H6, C4H8 cùng là anken nên có công thức chung là CnH2n
2CO + O2 → 2CO2↑ (1)
x → x (mol)
2H2 + O2 → 2H2O (2)
y → y (mol)
CnH2n + O2 → nCO2 + 2nH2O (3)
Sản phẩm cháy thu được gồm có CO2 và H2O.
Khi hấp thụ vào dd Ca(OH)2: 0,04 mol thu được dung dịch Y, thêm từ từ Ba(OH)2 vào dung dịch Y thu được kết tủa của các ion kim loại => CO2 phản ứng với Ca(OH)2 theo phương trình:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (4)
CO2 + Ca(OH)2 → Ca(HCO3)2 + H2O (5)
Dd Y chứa Ca(HCO3)2
BaCl2 + Ca(HCO3)2 → CaCO3↓ + BaCO3↓ + H2O (6)
m1 = mCaCO3(4)
m2 = mCaCO3(5) + mBaCO3
=> m1 + m2 = ∑ mCaCO3↓ + mBaCO3 = 6,955 (g) (*)
BTNT Ca: => ∑nCaCO3↓ = ∑ nCa(OH)2 (4+5) = 0,04 (mol)
Từ (*)

=> nCaCO3(6) = nBaCO3 = 0,015 (mol)
=> nCaCO3(4) = ∑nCa(OH)2 – nBaCO3 = 0,04 – 0,015 = 0,025 (mol)
BTNT C => ∑ nCO2 = ∑ nCaCO3 + nBaCO3 = 0,04 + 0,015 = 0,055 (mol)
Khối lượng dd Y tăng 0,82 gam so với dd Ca(OH)2 ban đầu
=> mCO2 + mH2O – mCaCO3(4) = 0,82
=> mH2O = 0,82 + 0,025.100 – 0,055.44 = 0,9 (g)
=> nH2O = 0,9 : 18 = 0,05 (mol)
BTKL ta có: mhhX + mO2 = mCO2 + mH2O
=> mO2 = 0,055.44 + 0,9 – 0,92 = 2,4 (g) => nO2 = 0,075 (mol)
BTNT O: nO( trong CO) + 2nO2 = 2nCO2 + nH2O
=> nO( trong CO) = 2.0,055 + 0,05 – 0,075.2 = 0,01 (mol) => nCO = 0,01 (mol)
Từ PTHH (1), (2), (3) ta thấy khi đốt cháy CnH2n luôn cho nH2O = nCO2 => sự chênh lệch mol CO2 và mol H2O là do đốt cháy CO và H2
=> nCO2 – nH2O = x – y = 0,055 – 0,05 = 0,005 (mol)
Mặt khác: nCO – nH2 = x – y = 0,005 (mol)
=> nH2 = nCO – 0,005= 0,01 – 0,005 = 0,055 (mol)
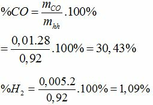

Đáp án A
Ta có: n C a C O 3 = 2/100 = 0,02 mol
mdung dịch tăng= m C O 2 - m C a C O 3
→ m C O 2 = 4,16 + 2 = 6,16 gam
→ n C O 2 = 0,14 mol
→ V C O 2 = 0,14.22,4 = 3,136 lít

Đáp án C
· Phần 1 qua Ca(OH)2 dư:
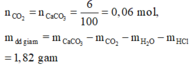
![]() Không khí bị hấp thụ là N2:
Không khí bị hấp thụ là N2:
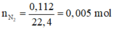
·Phần 2: Kết tủa thu được là AgCl
![]()
![]()
![]()
Vì
![]()
trong phần 1 có
![]()
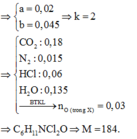
Vậy khi đốt cháy 5,52 gam X tạo ra 0,18 mol CO2; 0,135 mol H2O; 0,015 mol N2; 0,06 mol HCl
· Áp dụng định luật bảo toàn khối lượng có:
= 44.0,18 + 18.0,135 + 28.0,015 + 36,5.0,06 – 5,52 = 7,44 gam
![]()
· Áp dụng định luật bảo toàn nguyên tố O có:
nO(X) = 2.0,18 + 0,135 – 2.0,2325 = 0,03 mol

X có công thức C6H11ONCl2. Vậy MX = 184
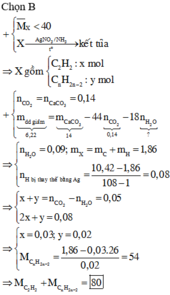

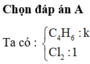
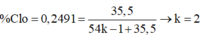


Ta có :
\(\Delta m\left(t\text{ă}ng\right)=mCO2\left(th\text{ê}m-v\text{ào}\right)-mkt=1,82=>mCO2=4+1,82=5,82\left(g\right)\)
vậy...