Hỗn hợp X gồm Fe, Cu và Fe3O4 (trong X, các kim loại có số mol bằng nhau). Hoà tan hoàn toàn
9,52 gam X trong dung dịch HNO3 (đặc, nóng, dư), thu được 6,944 lít khí NO2 duy nhất (đktc, không có sản
phẩm khử nào khác) và dung dịch Y. Tính % khối lượng của oxi trong X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
![]() Þ M không tác dụng được với NaOH.
Þ M không tác dụng được với NaOH.
Từ đó suy ra: ![]()
![]() (với n là hoá trị của M)
(với n là hoá trị của M)
Mà ![]() Từ (1), (2) suy ra M = 56 (Fe)
Từ (1), (2) suy ra M = 56 (Fe)
Vậy tính chất của M là không tan được trong dung dịch H2SO4 đặc, nguội.

Ta đặt: nNO= x mol; nNO2= y mol
Ta có : nY= x+y= 6,72/22,4= 0,3 mol
mY= 30x+ 46y= nY.MY= 0,3.19.2
Giải hệ có x= 0,15 và y= 0,15
Đặt nFe= a mol ; nCu= b mol
QT cho e:
Fe → Fe3++ 3e
a 3a mol
Cu → Cu2++ 2e
b 2b mol
QT nhận e:
N+5+ 3e→ NO
0,45 0,15
N+5+ 1e→ NO2
0,15 0,15
Theo ĐL bảo toàn e có: ne cho= ne nhận nên 3a+2b= 0,45+ 0,15= 0,60
Mặt khác mkim loại= 56a+ 64b= 15,2
Giải hệ trên có a= 0,1, b= 0,15 →%mFe=36,84%
Đáp án C

Đáp án D
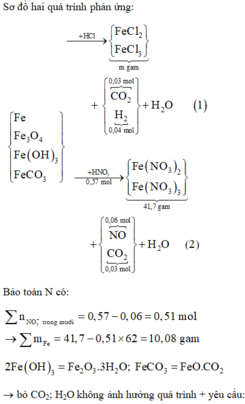
Sơ đồ hai quá trình phản ứng:
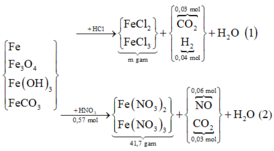
Bảo toàn N có:
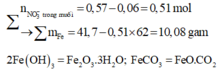
® bỏ CO2; H2O không ảnh hưởng quá trình + yêu cầu:
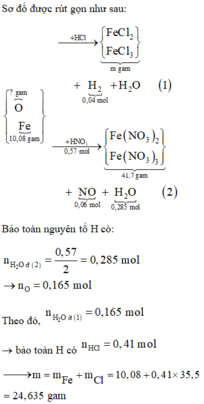
Sơ đồ được rút gọn như sau:
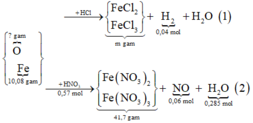
Bảo toàn nguyên tố H có:
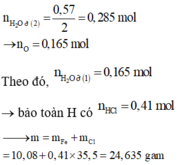

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)

Chọn đáp án D
gt ⇒ nFe = nMg = nCu = 0,1 mol || N2 = nNO2 ⇒ ghép: N2 + NO2 = N3O2 = N2O.NO = N2O + NO.
► Quy hỗn hợp khí về N2O và NO với số mol x và y || nkhí = x + y = 0,12 mol. HNO3 dư ⇒ Fe lên +3.
● mFe(NO3)3 + mMg(NO3)2 + mCu(NO3)2 = 0,1 × 242 + 0,1 × 148 + 0,1 × 188 = 57,8(g) < 58,8(g).
⇒ chứa muối NH4NO3 ⇒ nNH4NO3 = (58,8 - 57,8) ÷ 80 = 0,0125 mol. Bảo toàn electron:
3nFe + 2nMg + 2nCu = 8nN2O + 3nNO + 8NH4NO3 ⇒ 8x + 3y = 0,6 mol ||⇒ x = 0,048 mol; y = 0,072 mol.
► nHNO3 = 10nN2O + 4nNO + 10nNH4NO3 = 0,893 mol ⇒ chọn D.

gt ⇒ nFe = nMg = nCu = 0,1 mol
N2 = nNO2 ⇒ ghép: N2 + NO2 = N3O2 = N2O.NO = N2O + NO.
► Quy hỗn hợp khí về N2O và NO với số mol x và y
nkhí = x + y = 0,12 mol. HNO3 dư ⇒ Fe lên +3.
● mFe(NO3)3 + mMg(NO3)2 + mCu(NO3)2 = 0,1 × 242 + 0,1 × 148 + 0,1 × 188 = 57,8(g) < 58,8(g).
⇒ chứa muối NH4NO3 ⇒ nNH4NO3 = (58,8 - 57,8) ÷ 80 = 0,0125 mol. Bảo toàn electron:
3nFe + 2nMg + 2nCu = 8nN2O + 3nNO + 8NH4NO3 ⇒ 8x + 3y = 0,6 mol
⇒ x = 0,048 mol; y = 0,072 mol.
► nHNO3 = 10nN2O + 4nNO + 10nNH4NO3 = 0,893 mol
Đáp án D

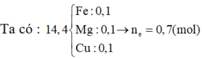
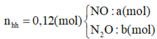
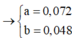
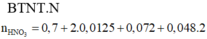
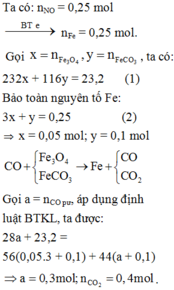
Gọi $n_{Fe} = n_{Cu} = a(mol) ; n_{Fe_3O_4} = b(mol)$
$\Rightarrow 56a + 64a + 232b = 9,52(1)$
$n_{NO_2} = \dfrac{6,944}{22,4} = 0,31(mol)$
Bảo toàn electron : $3a + 2a + b = 0,31(2)$
Từ (1)(2) suy ra a = 0,06 ; b = 0,01
$\%m_O = \dfrac{0,01.4.16}{9,52}.100\% = 6,722\%$
Quy đổi hỗn hợp thành : Fe ( x mol) , Cu ( x mol ) , O ( y mol )
\(m_X=56x+64x+16y=9.52\left(g\right)\left(1\right)\)
Bảo toàn e :
\(3x+2x=0.31+2y\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.075,y=0.0325\)
\(\%O=\dfrac{0.0325\cdot16}{9.52}\cdot100\%=5.46\%\)