mấy bạn ơi giúp mình bài này với
B1: Hoà 10g hỗn hợp X gồm Mg, Zn, Cu vào dd H2SO4 dư. SPU thu đc 5,152 lít khí H2(đktc), đồng thời thấy trong dung dịch có 1,2g chất rắn không tan. Tính phần trăm về khối lượng của mỗi kim loại trong hỗn hợp X và khối lượng H2SO4 đã tham gia phản ứng
B2: Nung hoàn toàn m1 (g) hỗn hợp X gồm MgCO3 và ZnCO3 thu được 2,016 lít khí và m2 (g) chất rắn Z. Cho Z tác dụng vừa đủ với m3 (g) dd HCl 14,678% thu đc dd Y. Cô gạn dd Y thu được 10,19g muối
a) tính các giá trị m1, m2, m3 (m3 làm tròn đến 2 chữ số thập phân)
b) tính nồng độ phần trăm các chất trong dung dịch Y
B3: Hỗn hợp Mg, Fe có khối lượng m gam đc hoà tan hoàn tàn bởi dd HCl. Dd thu đc td với dd NaOH dư . Kết tủa sinh ra phản ứng đem nung trong không khí đến khối lượng không giảm đi a gam so với trc khi nung
a) Xác định % về khối lượng mỗi kim loại theo m, a
b) áp dụng với m=8g, a=2,8g

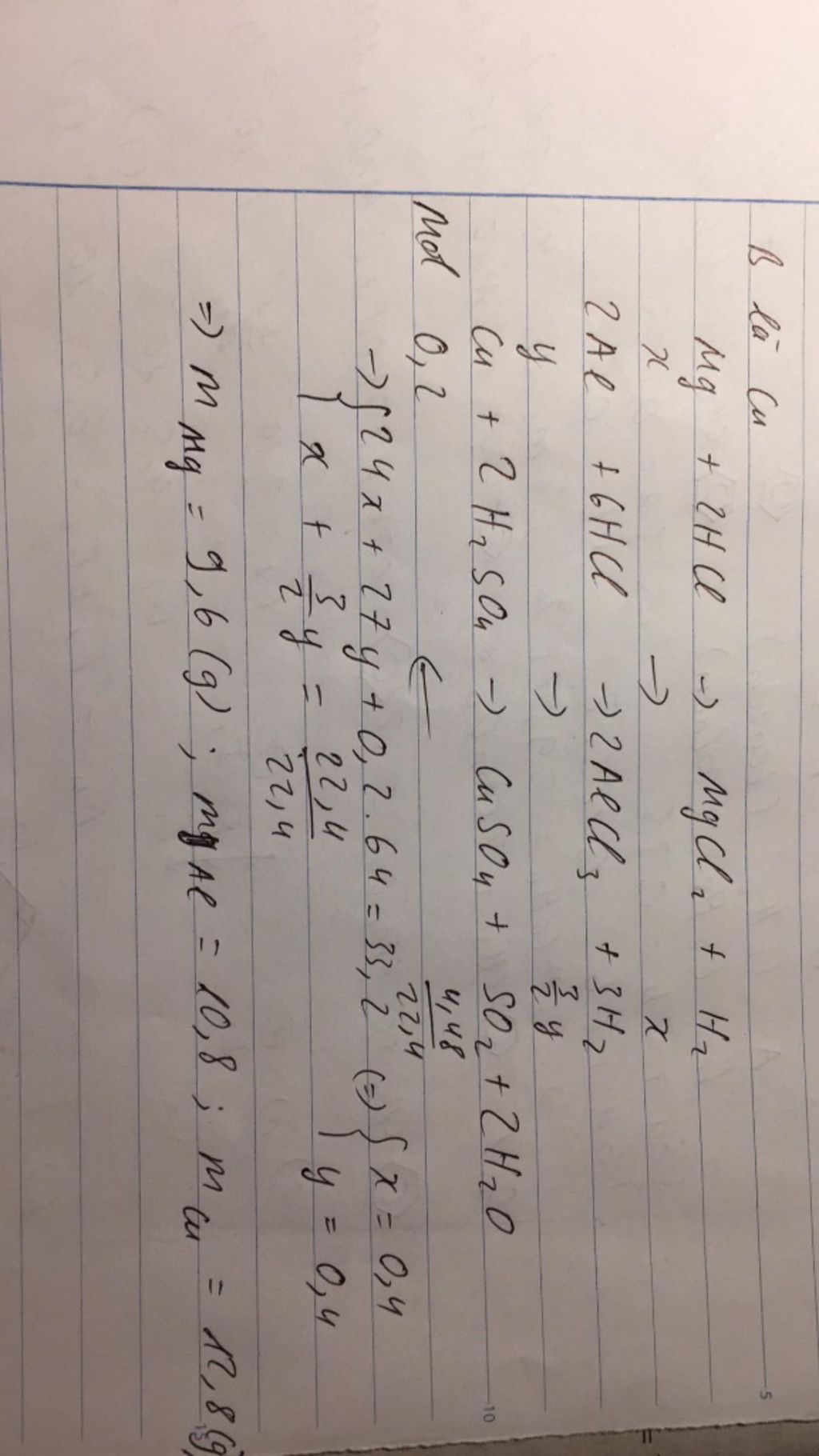

http://violet.vn/thcs-levanhien-tuyenquang/present/show/entry_id/8933448
bài 3 bn có thể tham khảo đây còn mik k hiểu chỗ a lắm nên k làm dc
bài 1:
Chất rắn không tan là Cu => mCu = 1,2(g)
\(m_{Mg}+m_{Zn}=m_X-m_{Cu}=10-1,2=8,8\left(g\right)\)
\(n_{H_2}=0,23\left(mol\right)\)
\(Mg+H_2SO_4-->MgSO_4+H_2\)
x..............x......................x...................x
\(Zn+H_2SO_4-->ZnSO_4+H_2\)
y............y.........................y..............y
\(\left\{{}\begin{matrix}24x+65y=8,8\\x+y=0,23\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,15\\y=0,08\end{matrix}\right.\)
\(\%Cu=\dfrac{1,2}{10}.100\%=12\%\)
\(\%Mg=\dfrac{0,15.24}{10}.100\%=36\%\)
\(\%Zn=100\%-36\%-12\%=52\%\)
\(m_{H_2SO_4\left(pu\right)}=\left(0,15+0,08\right).98=22,54\left(g\right)\)