Ngâm một lá sắt có khối lượng 2,5 gam trong 25 ml dung dịch CuSO4 15% có khối lượng riêng là 1,12 g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô thì cân nặng 2,58 gam.
a) Hãy viết phương trình hoá học.
b) Tính nồng độ phần trăm của các chất trong dung dịch sau phản ứng.

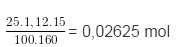


Fe + CuSO4 \(\rightarrow\) FeSO4 + Cu
x..........x..................x.............x
mFe tăng = mCu - mFe
<=> 64x - 56x = 2,58 - 2,5 = 0,08
<=> 8x = 0,08
<=> x = 0,01
Theo đề bài
mCuSO4 = 15%.( 25.1,12 ) = 4,2
=> nCuSO4 = 0,02625 mol
Ta có
0,01/1 < 0,02625
=> Dư CuSO4, n dư = 0,02625 - 0,01 = 0,01625
=> mCuSO4 dư = 0,01625.160 = 2,6
Theo phản ứng mFeSO4 = 0,01.152 = 1,52 g
Theo định luật bảo toàn khối lượng:
mdd sau phản ứng = 0,01.56 + 1,12.25 - 0,08 = 28,48
% FeSO4 = 1,52 : 28,48 . 100 = 5,34%
% CuSO4 = 2,6 : 28,48 . 100 = 9,13%
a) PTHH : Fe + CuSO4 \(\rightarrow\) FeSO4 + Cu (1)
b) Gọi số mol của Fe là x (mol) (x nguyên dương )
Theo (1) : nCu =nCuSO4=nFe = x (mol)
\(\Rightarrow\) mFe ( thu được sau phản ứng ) =56x
mCu = 64x
Khối lượng tăng lên sau phản ứng là : 2,58 - 2,5 = 0,08 (g)
Theo bài ra ta có phương trình : 64x -56x = 0,08
\(\Rightarrow\) x= 0,01
mddCuSO4 = 1,12 . 25 = 28 (g) \(\Rightarrow\) mCuSO4 = \(\dfrac{28.15}{100}\) = 4,2 (g)
nCuSO4 = \(\dfrac{4,2}{160}\) =0,02625 (mol)
\(\Rightarrow\) CuSO4 dư
nCuSO4(dư) = nCuSO4( đề bài ) - nCuSO4( phản ứng )
= 0,2625-0,1=0,1625 (mol)
mCuSO4(dư) = 0,1625 . 160 =26 (g)
Khối lượng dung dịch sau phản ứng = mddCuSO4 = 28 (g)
C%CuSO4(dư) = \(\dfrac{26}{28}.100\)% = 92,86 %