Tính thể tích khí hiđro và khí oxi( ở đktc) cần tác dụng với nhau để tạo ra được 1,8 gam nước.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2o}=\dfrac{1,8}{18}=0,1\left(mol\right)\\
pthh:2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,1 0,1
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
PTHH: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,1<--0,05<--0,1
\(\rightarrow\left\{{}\begin{matrix}V_{O_2}=0,05.22,4=1,12\left(l\right)\\V_{H_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)

\(PTHH:2H_2+O_2\rightarrow2H_2O\)
Số mol của 3,6 gam nc là:
\(n_{H_2O}=\dfrac{m}{M}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Thể tích khí Oxi là:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Thể tích khí hidro là:
\(V_{H_2}=n.22,4=0,2.22,4=4,48\left(l\right)\)

Ta có: \(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
_____0,3_____0,9___0,6____0,9 (mol)
a, \(m_{Fe}=0,6.56=33,6\left(g\right)\)
b, \(V_{H_2}=0,9.22,4=20,16\left(l\right)\)
c, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2O}=0,9\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,9.22,4=20,16\left(l\right)\)

Số mol nước tạo thành là:
nH2OnH2O = 1,8/18 = 0,1 (mol)
Phương trình phản ứng:
2H2 + O2 → 2H2O
2 mol 1 mol 2 mol
0,1 mol 0,05 mol 0,1 mol
Thể tích khí hidro tham gia phản ứng:
V = 22,4 x 0,1 = 2,24 (lít)
Thể tích khí oxi tham gia phản ứng:
V = 22,4 x 0,05 = 1,12 (lít)
- cái này là Hóa 8 mà sao cho dzô thể loại toán 7 vậy má =))

Số mol của 4,48 lít H2:
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
tỉ lệ: 2 : 1 : 2
0,2-> 0,1 : 0,2( mol)
a/ số gam của 0,2 mol nước:
\(m_{H_2O}=n.M=0,2.=3,6\left(g\right)\)
b/ thể tích của 0,1 mol khí O2:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)

1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)

nH2O = 7,2/18 = 0,4 mol
2H2 + O2 ➝ 2H2O
0,4 0,2 0,4 (mol)
VH2 = 0,4.22,4 = 8,96 lít
VO2 = 0,2.22,4 = 4,48 lít

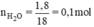
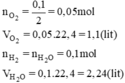
nH2O = 1,8 / 18 = 0,1 mol
Phương trình phản ứng:
2H2 + O2 —> 2H2O
2 mol 1 mol 2 mol
y mol x mol <— 0,1 mol
x = 0,1 / 2 = 0,05 mol -> VO2 = 0,05 x 22,4 = 1,12 lít
y = (2 x 0,1) / 2 = 0,1 mol -> VH2= 0,1 x 22,4 = 2,24 lít.
Ta có nH2O = \(\dfrac{1,8}{18}\) = 0,1 ( mol )
H2 + \(\dfrac{1}{2}\)O2 \(\rightarrow\) H2O
0,1.....0,05.......0,1
=> VH2 = 22,4 . 0,1 = 2,24 ( lít )
=> VO2 = 22,4 . 0,05 = 1,12 ( lít )