Nhiệt phân hoàn toàn 10,1 gam một muối nitrat RNO3 đến khi phản ứng xảy ra hoàn toàn thu được 8,5 gam một chất rắn. Hãy xác định công thức của muối:
A. KNO3 B. NaNO3 C. LiNO3 D. AgNO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi Công thức của muối là XNO3
XNO3 (nhiệt độ)----> XNO2+ 1/2 O2
Khối lượng muối giảm là khối lượng của O2
suy ra m(O2)=15,84%. 10,1=1,6 suy ra n(O2)=0.05
suy ra n(muối)=0.1 suy ra M(muối)= 10,1/0.1=101
suy ra X=101-62=39 suy ra X là Kali
V(O2)=0.05.22,4=1,12 l

.
Nhận thấy nCO2 = nH2O = 0,4 mol
=> este no đơn chức
=> số C = 0,4 : 0,1 = 4
=> C4H8O2
b.
R1COOR2 + NaOH → R1COONa + R2OH
0,1 → 0,1 0,1
=> Chất rắn gồm R1COONa: 0,1 và NaOH dư: 0,1 mol (m rắn = 13,6g)
=> R1 = 29 (C2H5)
=> X: C2H5COOCH3

Đáp án C
Xét các trường hợp:
+) Nhiệt phân R(NO3)n tạo muối nitrit:
R ( N O 3 ) 2 → t 0 R ( N O 2 ) 2 + n 2 O 2
Khi đó khối lượng chất rắn giảm là khối lượng O2.
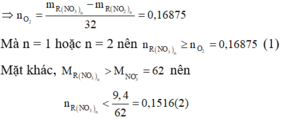
Từ (1) và (2) ta có trường hợp này không thỏa mãn.
+) Nhiệt phân R(NO3)n tạo oxit kim loại với hóa trị không đổi:
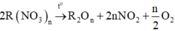
Khi đó khối lượng chất rắn giảm là khối lượng của hỗn hợp khí gồm NO2 và O2.

Vậy công thức của muối là R(NO3)n.

Đáp án A
Căn cứ vào 4 đáp án, ta nhận thấy cả 4 kim loại tương ứng với 4 đáp án đều rơi vào trường hợp nhiệt phân muối nitrat tạo oxit kim loại. Khối lượng chất rắn giảm là khối lượng của hỗn hợp khí gồm NO2 và O2.
Có hai trường hợp xảy ra:
+) Hóa trị của M trong oxit sản phẩm và tỏng muối là như nhau. Khi đó:
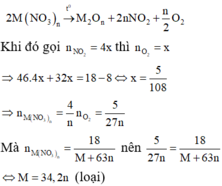
+) Do đó trường hợp thỏa mãn là hóa trị của M trong oxit và muối khác nhau.
Trong 4 đáp án chỉ có kim loại Fe thỏa mãn (muối thỏa mãn là Fe(NO3)2).

Gọi CTHH của oxit sắt là FexOy.
PT: \(ZnO+H_2\underrightarrow{t^o}Zn+H_2O\)
\(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
B gồm: Zn và Fe.
Gọi: \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\) ⇒ 65a + 56b = 17,7 (1)
Theo PT: \(n_{H_2}=n_{Zn}+n_{Fe}=a+b=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{ZnO}=n_{Zn}=0,1\left(mol\right)\\n_{Fe_xO_y}=\dfrac{1}{x}n_{Fe}=\dfrac{0,2}{x}\left(mol\right)\end{matrix}\right.\)
Có: mZnO + mFexOy = 24,1 ⇒ mFexOy = 24,1 - 0,1.81 = 16 (g)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{16}{\dfrac{0,2}{x}}=80x\left(g/mol\right)\)
\(\Rightarrow56x+16y=80x\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: CTHH cần tìm là Fe2O3.
\(\Rightarrow\left\{{}\begin{matrix}\%m_{ZnO}=\dfrac{0,1.81}{24,1}.100\%\approx33,61\%\\\%m_{Fe_2O_3}\approx66,39\%\end{matrix}\right.\)

Đáp án A
Gọi công thức của muối đem nhiệt phân là M(NO3)n.
Ta sẽ sử dụng PP loại trừ để tìm ra đáp án đúng.
* Nếu chất rắn thu được là muối nitrit thì khối lượng chất rắn giảm là khối lượng của O2. Khi đó
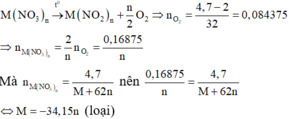
* Nếu chất rắn thu được là kim loại thì gồm khối lượng chất rắm giảm gồm NO2 và O2.
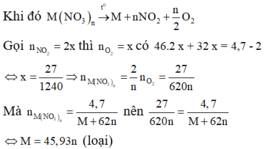
Vậy chất rắn thu được là oxit kim loại.
Chú ý: Khi thực hiện phương pháp loại trừ với bài toán này, chúng ta thực hiện tính toán đối với trường hợp chất rắn là muối nitrit và kim loại trước vì với trường hợp tạo oxit kim loại thì hóa trị của kim loại có thể thay đổi hoặc không nên quá trình tính toán sẽ phức tạp hơn.
Nếu kết quả tính toán rơi vào 1 trong 2 trường hợp đem tính toán thì kết luận đáp án là 1 trong 2 trường hợp đó, còn nếu cả 2 trường hợp đều không tìm được ra kim loại thỏa mãn thì đáp án là trường hợp còn lại với chất rắn là oxit kim loại vì khi nhiệt phân muối nitrat, sản phẩm rắn sau phản ứng thu được chỉ có thể là muối nitrit, oxit kim loại hoặc kim loại.
Giả sử R là kim loại kiềm.
$2RNO_3 \xrightarrow{t^o} 2RNO_2 + O_2$
Theo PTHH :
$n_{RNO_3} = n_{RNO_2}$
$\Rightarrow \dfrac{10,1}{R + 62} = \dfrac{8,5}{R + 46}$
$\Rightarrow R = 39(Kali)$
Đáp án A