1. Cho hỗn hợp Mg và MgCO3 tác dụng vừa đủ với dung dịch HCl 0,5M được dd A. Dẫn khí tạo thành lội qua dd Ca(OH)2 dư thì thu được 10g kết tủa và còn 2,8 lít khí không màu (đktc) .
a, Tính thành phần trăm về khối lượng của mỗi chất.
b, Tính CM các chất trong A .
2. Hòa tan hoàn toàn một lượng hỗn hợp A gồm CaO , CaCO3 bằng dd HCl vừa đủ , thu được dd B và 4,48 lít khí CO2 (ở đktc) . Đem cô cạn dd B thu được 66,6g muối khan.
a, Xác định khối lượng mỗi chất có trong hỗn hợp A.
b, Xác định khối lượng dd HCl 7,3% cần dùng để hòa tan vừa hết lượng hỗn hợp A nêu trên.


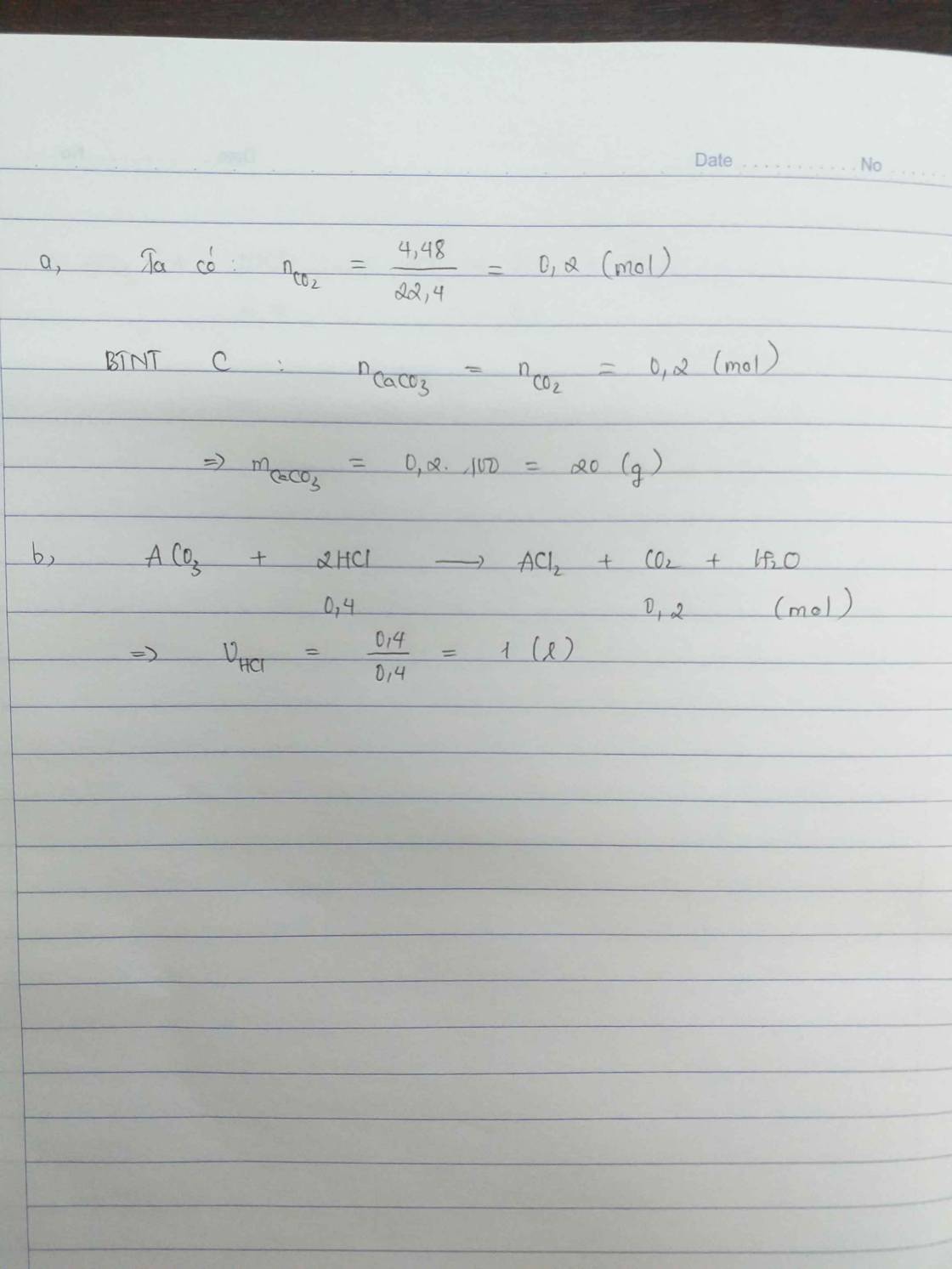

Bài 2 :
PTHH :
CaO + 2HCl ----> CaCl2 + H2 (PT1)
CaCO3 + 2HCl ------> CaCl2 + CO2 + H2O (PT2)
Phản ứng hoàn toàn :
Ta có : nCO2 = 4,48 : 22,4 = 0,2 (mol)
=> nCaCO3 = 0,2 (mol) => nCaCl2 (PT2) = 0,2 (mol)
=> mCaCO3 = 0,2 . (40 + 12 + 48) = 20 (g)
Ta thấy : dd B có chứa CaCl2 của PT1 và PT2
Sau khi cô cạn dung dịch B thì dd còn lại muối CaCl2
Ta có : mCaCl2 (PT2) = 0,2 . (40 + 71) =22,2 (g)
=> 22,2 + mCaCl2 (PT1) = 66,6
=> mCaCl2 (PT1) = 44,4 (g)
=> nCaCl2 (PT1) = 44,4 : (40 + 71) = 0,4 (mol)
=> nCaO = 0,4 (mol)
=> mCaO = 0,4 . (40 + 16) = 22,4 (g)
b)
nHCl (cần dùng) = nHCl (PT1) + nHCl (PT2) = 0,8 + 0,4 = 1,2 (mol)
=> mHCl (cần dùng) = 1,2 . 36,5 = 43,8 (g)
=> mdd HCl 7,3% = 43,8 : 7,3% = 600(g)
Bài 1 :
Ta có PTHH :
(1) \(Mg+2HCl->MgCl2+H2\uparrow\)
(2) \(MgCO3+2HCl->MgCl2+H2O+CO2\uparrow\)
Vì khí H2 không làm đục nước vôi trong Ca(OH)2 nên nó sẽ không phản ứng
=> khí không màu sau p/ư là H2 => VH2 = 2,8(l) => nH2 = \(\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
=> nMg = 0,125 mol
Ta có : mkt = mCaCO3 = 10(g) => nCaCO3 = 0,1(mol)
Ta có PTHH 3 :
\(CO2+Ca\left(OH\right)2->CaCO3+H2O\)
0,1mol................................0,1mol
=> nCO2 = 0,1(mol)
=> nMgCO3 = 0,1 (mol)
a) Ta có :
%mMg = \(\dfrac{0,125.24}{0,125.24+0,1.84}.100\%\approx26,32\%\)
%mMgCO3 = 100% - 26,32% = 73,68%
b) Ta có : nHCl(1) = 2nH2 = 0,25 mol ; nCO2(2) = 2nCo2 = 0,2 mol
VddHCl = \(\dfrac{0,25+0,2}{0,5}=0,9\left(M\right)\)
Ta có : nMgCl2(1) = nH2 = 0,125 mol ; nMgCl2(2) = nCo2 = 0,1(mol)
Ta có : \(CM_{MgCl2}=\dfrac{0,125+0,1}{0,9}=0,25\left(M\right)\)
Bài 2 :
Theo đề bài ta có : nCo2 = \(\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Ta có PTHH :
(1) \(CaO+2HCl->CaCl2+H2O\)
(2) \(CaCO3+2HCl->CaCl2+H2O+CO2\uparrow\)
0,2mol..........0,4mol..........0,2mol................0,2mol
DD B thu được là CaCl2
a) Ta có :
mCaCl2(2) = 0,2.111 = 22,2(g)
=> mCaCl2(1) = 66,6 - 22,2 = 44,4(g)
Theo PTHH 1 ta có : nCaO = nCaCl2 = \(\dfrac{44,4}{111}=0,4\left(mol\right)\)
=> Khối lượng mỗi chất trong A là :
mCaO = 0,4.56 = 22,4(g)
mCaCO3 = 0,2.100 = 20(g)
b) ta có : nHCl(1) = 2nCaO = 2.0,4 = 0,8(mol)
=> nHCl = nHCl(1) + nHCl(2) = 0,8 + 0,2 = 1 mol
=> mddHCl = \(\dfrac{1.36,5}{7,3}.100=500\left(g\right)\)
Vậy..............