Dùng H2 dư để khử hoàn toàn m gam bột sắt oxit, thu được 5,4 gam nước. Hoà tan toàn bộ lượng sắt thu được ở trên bằng dung dịch HCl dư thì thu được 25,4 gam muối. Tìm công thức oxit sắt ? Tính giá trị của M ?
Các bạn giải dùm mik nhanh nha !!!!! Mình cảm ơn

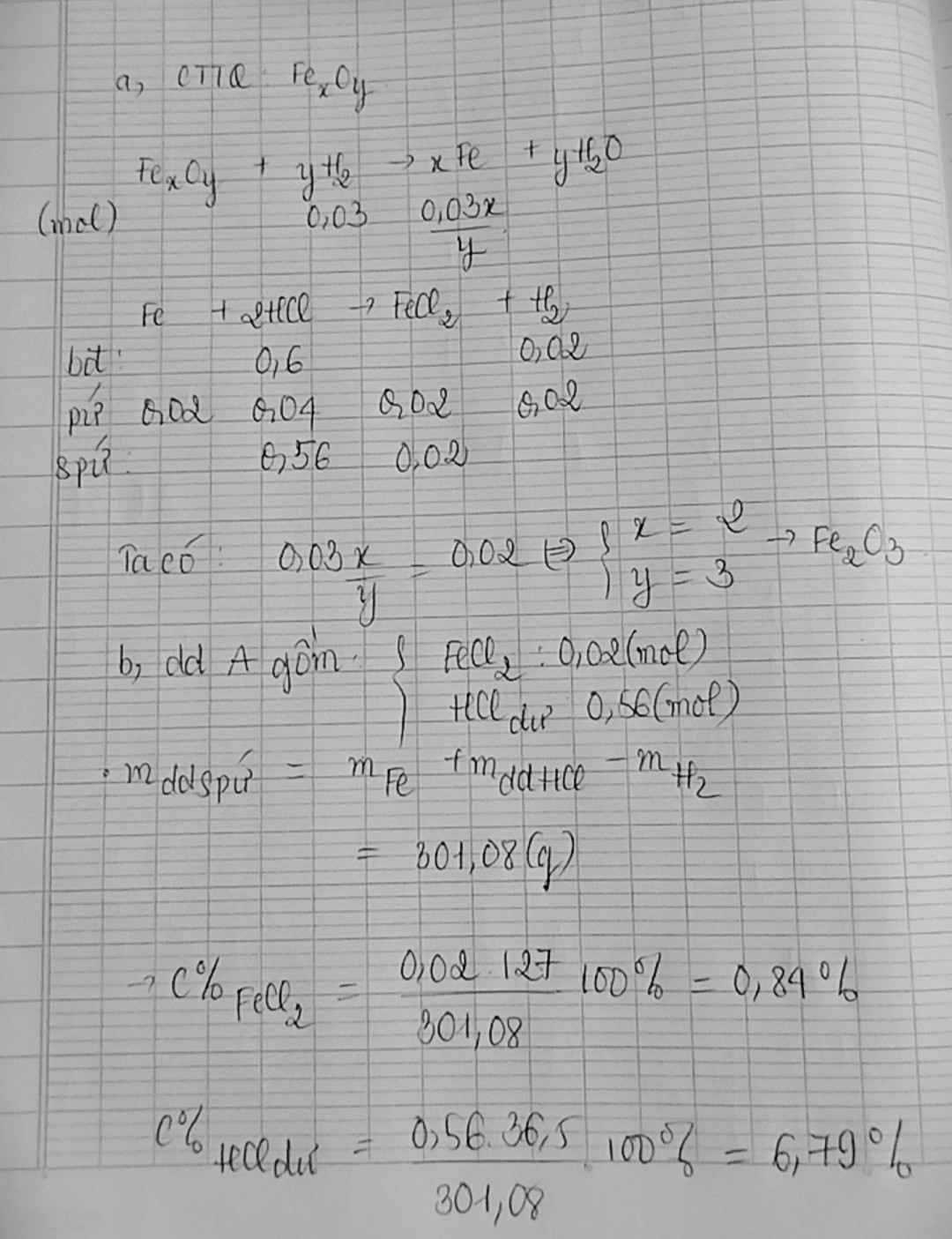
Gọi công thức hóa học của oxit sắt là FexOy
PTHH FexOy + y H2 ---> xFe + yH2O (1)
PTHH Fe + 2HCl ---> FeCl2 + H2(khí) (2)
Có n FeCl2 =25,4/127=0,2 (mol)
Từ (2) => n Fe = n FeCl2 = 0,2 (mol)
Từ (1) => n FexOy = \(\dfrac{n_{ }Fe}{x}\) = 0,2/x (mol) (*)
Có n H2O= 5,4/18=0,3 (mol)
Từ (1) => n FexOy = \(\dfrac{nH_2O}{y}\) = 0,3/y (mol) (**)
Từ (*) và (**) => \(\dfrac{0,2}{x}=\dfrac{0,3}{y}\) => x/y = 2/3
Vậy CTHH của oxit sắt là Fe2O3
Có n Fe2O3 = 0,3/y=0,3/3=0,1 (mol)
=> m Fe2O3 = 0,1.160=16 (g)