Dùng 6.72l CO khử hoàn toàn 8g oxit kim loại M thu được kim loại và hỗn hợp khí B có tỉ khối so với H2 là 18. Mặt khác toàn bộ lượng kim loại sinh ra hòa tan hoàn toàn và dd HCl được 2.24l H2 (đktc). Tìm M và công thức oxit.
Giúp mk vs ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n CO = 6,72/22,4 = 0,3(mol)
n H2 = 2,24/22,4 = 0,1(mol)
B gồm : CO(x mol) ; CO2(y mol)
M B = 18.2 = 36
x + y = 0,3
28x + 44y = 36(x + y)
=> x = y = 0,15
$CO + O_{oxit} \to CO_2$
n O(oxit) = n CO2 = 0,15(mol)
=> m M = 8 - 0,15.16 = 5,6(gam)
n là hóa trị của M
$2M + 2HCl \to 2MCl_n + nH_2$
n M = 2/n . nH2 = 0,2/n (mol)
=> 0,2/n . M = 5,6
=> M = 28n
Với n = 2 thì M = 56(Fe)
n Fe = 5,6/56 = 0,1(mol)
n Fe / n O = 0,1/0,15 = 2/3 . Vậy oxit là Fe2O3

PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ

Ta có: \(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
⇒ n O (trong oxit) = 0,45 (mol)
Có: m oxit = mM + mO ⇒ mM = 24 - 0,45.16 = 16,8 (g)
Giả sử kim loại M có hóa trị n khi tác dụng với H2SO4.
PT: \(2M+nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nH_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,6}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{16,8}{\dfrac{0,6}{n}}=28n\)
Với n = 1 ⇒ MM = 28 (loại)
Với n = 2 ⇒ MM = 56 (nhận)
Với n = 3 ⇒ MM = 84 (loại)
⇒ M là Fe. ⇒ Oxit cần tìm là FexOy.
PT: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
Theo PT: \(n_{Fe_xO_y}=\dfrac{1}{y}n_{H_2O}=\dfrac{0,45}{y}\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{24}{\dfrac{0,45}{y}}=\dfrac{160}{3}y\)
\(\Rightarrow56x+16y=\dfrac{160}{3}y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: Oxit đó là Fe2O3.
Bạn tham khảo nhé!

nH2 (khử)= 1,344/22,4= 0,06 mol
nH2 (axit)= 1,008/22,4= 0,045 mol
nH2(khử)= nO(bị khử)
=> mO (bị khử)= 0,06.16= 0,96g
=> mM= 3,48-0,96= 2,52g
2M+ 2nHCl -> 2MCln+ nH2
nH2 (axit)= 0,045 mol => nM= 0,09/n mol
=> MM= 28n
n=2 => M=56. Vậy M là Fe
Mặt khác:
nFe= nH2(axit)= 0,045 mol
nO (bị khử)= 0,06 mol
nFe : nO= 3:4
Vậy oxit sắt là Fe3O4

CTHH: A2Oy
\(n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\)
PTHH: A2Oy + yCO --to--> 2A + yCO2
\(\dfrac{0,05}{y}\)<---------------------0,05
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,05<---0,05
=> \(M_{A_2O_y}=2.M_A+16y=\dfrac{4}{\dfrac{0,05}{y}}\)
=> \(M_A=32y\left(g/mol\right)\)
Xét y = 1 => MA = 32 (Loại)
Xét y = 2 => MA = 64 (Cu)
Vậy CTHH của oxit là CuO
dẫn X (chứa CO2 và CO dư) qua nước vôi trong (Ca(OH)2) thu được kết tủa là CaCO3 á :v

a)
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
n CO2 = n CaCO3 = 5/100 = 0,05(mol)
$CO + O_{oxit} \to CO_2$
n O(oxit) = n CO2 = 0,05(mol)
CTHH của oxit : RxOy
=> n oxit = 0,05/y (mol)
=> (Rx + 16y).0,05/y = 4
<=> Rx = 64y
Với x = y = 1 thì R = 64(Cu)
Vậy oxit là CuO
b)
X gồm CO(a mol) và CO2(0,05 mol)
M X = 19.2 = 38
=> 28a + 0,05.44 = (a + 0,05).38
<=> a = 0,03
n CO = n CO2 + n CO dư = 0,08(mol)
=> V = 0,08.22,4 = 1,792 lít
%m CO = 0,03.28/(0,03.28 + 0,05.44) .100% = 27,63%
%m CO2 = 100% -27,63% = 72,37%
\(n_{CaCO_3}=\dfrac{5}{100}=0.05\left(mol\right)\)
\(n_{CO_2}=0.05\left(mol\right)\)
\(n_{CO}=a\left(mol\right)\)
\(\overline{M}=\dfrac{28a+0.05\cdot44}{a+0.05}=19\cdot2=38\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow x=0.03\)
\(M_xO_y+yCO\underrightarrow{^{t^0}}xM+yCO_2\)
\(\dfrac{0.05}{y}.................0.05\)
\(M=\dfrac{4}{\dfrac{0.05}{y}}=80y\)
\(\Leftrightarrow xM+16y=80y\)
\(\Leftrightarrow xM=64y\)
\(x=y=1,M=64\)
\(CT:CuO\)
\(V_{CO}=\left(0.05+0.03\right)\cdot22.4=1.792\left(l\right)\)
\(\%m_{CO}=\dfrac{0.03\cdot28}{0.03\cdot28+0.05\cdot44}\cdot100\%=27.63\%\)
\(\%m_{CO_2}=72.37\%\)

Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
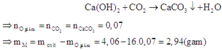
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
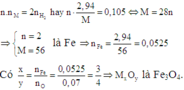
Đáp án D.
Fe2O3