Trộn m gam Ba và 8,1 gam bột kim loại Al , rồi cho vào một lượng H2O ( dư ) , sau phản ứng hoàn toàn có 2,7 gam chất rắn không tan . Khi trộn 2m gam Ba và 8,1 gam bột Al rồi cho vào H2O ( dư ) , sau phản ứng hoàn toàn thu được V lít khí H2 ( đktc ) . Tính giá trị của V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
+ TN 1 : Ba : x mol Al : 0 , 3 mol → H 2 O Ba ( AlO 2 ) 2 ⏟ x mol + Al d ¨ o ⏟ 0 , 1 mol + H 2 ↑ ⇒ 2 x + 0 , 1 = 0 , 3 ⇒ x = 0 , 1 . + TN 2 : Ba : 0 , 2 mol Al : 0 , 3 mol → H 2 O Ba ( AlO 2 ) 2 : 0 , 15 mol Ba ( OH ) 2 : 0 , 05 mol + H 2 ↑ ⇒ BTE : 0 , 2 . 2 + 0 , 3 . 3 = 2 n H 2 ⇒ n H 2 = 0 , 85 mol ⇒ V H 2 = 14 , 56 lít

Gọi $n_{Na} = a(mol)$
2Na + 2H2O → 2NaOH + H2
a...........................a..........0,5a.....(mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
..a...........a............................................1,5a....(mol)
Suy ra : $0,5a + 1,5a = \dfrac{3,36}{22,4} = 0,15 \Rightarrow a = 0,075$
Vậy :
$m = 0,075.23 + 0,075.27 + 1,35 = 5,1(gam)$
Gọi nNa=a(mol)���=�(���)
2Na + 2H2O → 2NaOH + H2
a...........................a..........0,5a.....(mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
..a...........a............................................1,5a....(mol)
Suy ra : 0,5a+1,5a=3,3622,4=0,15⇒a=0,0750,5�+1,5�=3,3622,4=0,15⇒�=0,075
Vậy :
m=0,075.23+0,075.27+1,35=5,1(gam)
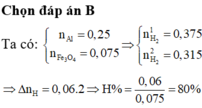


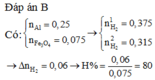
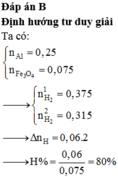

Ba + 2H2O --> Ba(OH)2 + H2
0,1 0,1
2Al + Ba(OH)2 + 2H2O --> Ba(AlO2)2 + 3H2
0,2 0,1
Vì TH1 ta thấy : khi cho hh vào H2O dư thì chắc chắn Ba tan hết => chất rắn còn lại là Al => Al dư còn Ba tác dụng hết => dựa vào số mol Al đã tác dụng thay vào để tính số mol Ba = 0,1 mol => m = 13,7 gam . Ta có TH 2 thì lấy 2m gam Ba nghĩa là lấy 27,4 gam Ba td với 8,1 gam Al thì tan hoàn toàn => số mol H2 được tính theo số mol Ba và Al :
Ba --> H2 Al --> 3/2 H2
0,2 0,2 0,3 0,45
=> tổng số mol H2 = 0,65 mol => V = 14,56 lít
nAl phản ứng = \(\dfrac{8,1-2,7}{27}=0,2\left(mol\right)\)
Ba + 2H2O -> Ba(OH)2 + H2
x-------------------x
Al + Ba(OH)2 + 2H2O -> Ba(AlO2)2 + 3H2
2x-----x
\(\Rightarrow2x=0,2\Rightarrow x=0,1\left(mol\right)\)
Khi trộn 2m gam Ba và 8,1 gam bột Al rồi cho vào H2O ( dư ) thì số mol Ba(OH)2 sinh ra là 0,2 mol \(\Rightarrow\) Al tan hết
\(n_{H_2}=n_{Ba}+1,5n_{Al}=0,2+1,5\cdot0,3=0,65\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,65\cdot22,4=14,56\left(l\right)\)
Vậy giá trị của V là 14,56 ( lít )