1. Tính nồng độ mol của dung dịch khi hòa tan 100g ZnSO4 vào 400g nước thu được dung dịch có khối lượng riêng D = 1,232g/ml.
2. Bằng phương pháp hóa học, nhận biết:
a. 3 dung dịch HCl, H2SO4, HNO3
b. 4 dung dịch CuCl2, Mg(NO3)2, NaOH, Fe2(SO4)3
c. 3 chất rắn Fe, Al, Cu
d. 3 chất rắn Ag, CuO, Fe chỉ dùng 1 thuốc thử
e. 4 chất rắn K, Ba, Na2O, P2O5
f. 4 chất khí CO2, N2, O2, Cl2

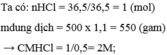
câu 1
\(n_{ZnSO_4}=\dfrac{100}{161}=0,62mol\)
khối lượng dung dịch thu được là : 100 + 400 =500 gam
thể tích dung dịch thu được là : \(V=\dfrac{m}{D}=\dfrac{500}{1,232}=405,8ml=0,4058lit\)
CM = 0,62/0,4058=1,5 M
Bài 1: Ta có: \(m_{ddthudc}=100+400=500\left(g\right)\\ V_{ddthudc}=\dfrac{m_{ddthudc}}{D_{ddthudc}}=\dfrac{500}{1,232}\approx405,844\left(ml\right)\approx0,405844\left(l\right)\)
\(n_{ZnSO_4}=\dfrac{100}{161}\approx0,621\left(mol\right)\)
=> \(C_{Mddthudc}=\dfrac{0,621}{0,405844}\approx1,5\left(M\right)\)