Hòa tan 16,25 gam kim loại A ( hóa trị 2) vào dung dịch HCl,phản ứng kết thúc thu được 5,6 lít khi hiđro ở đktc.
a.Hãy xác định kim loại A.
b.Nếu dùng lượng kim loại trên tác dụng hết với dung dịch H2SO4 thì thu được 5,04 lít khí hiđro ơt đktc.Tính hiệu suất phản ứng.

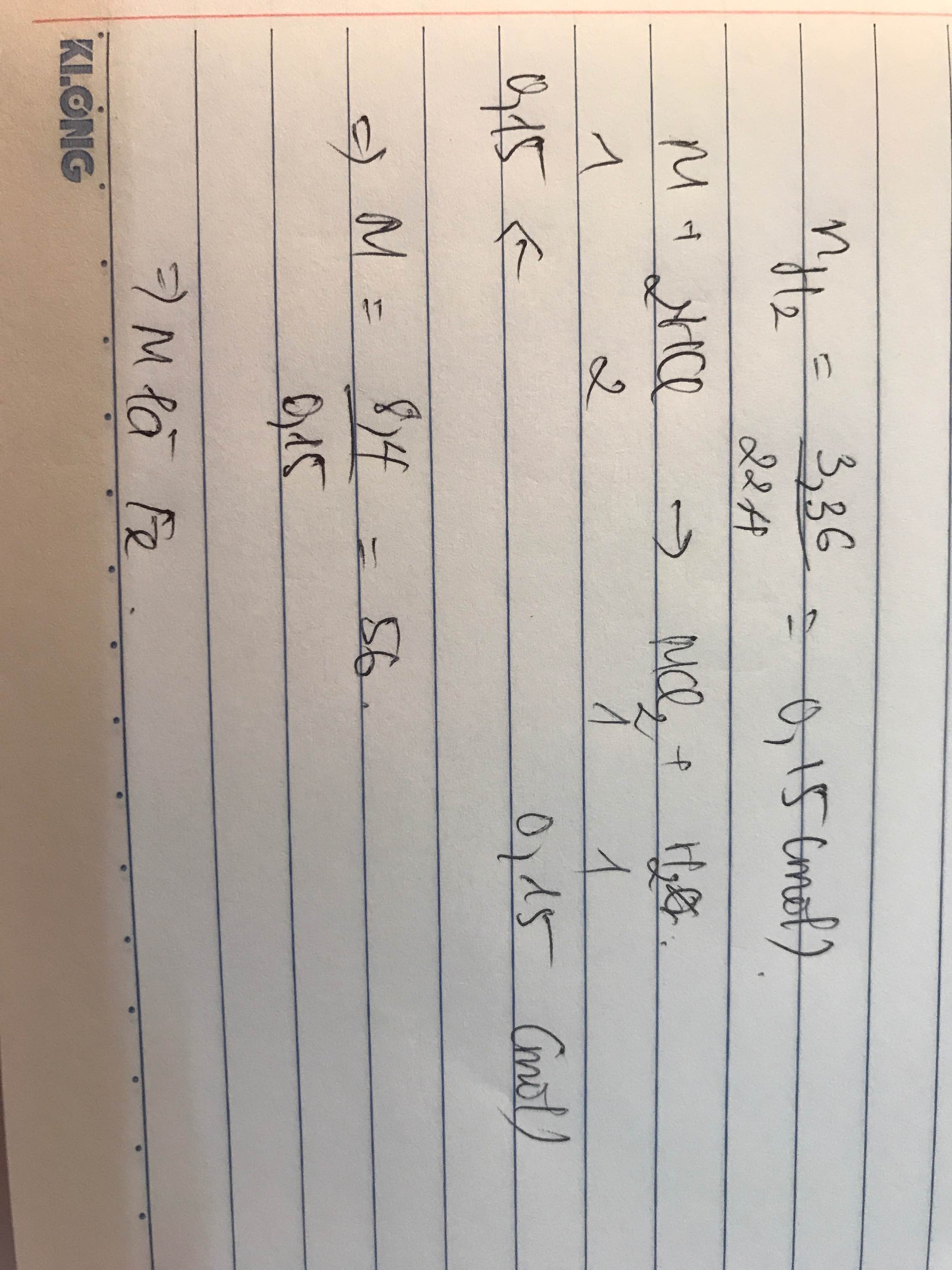
Ta có pthh 1
A + 2HCl \(\rightarrow\) ACl2 + H2
Theo đề bài ta có
nH2=\(\dfrac{5,6}{22,4}=0,25mol\)
a,Theo pthh 1
nA=nH2=0,25 mol
\(\Rightarrow\) Khối lượng mol của kim loại A là
MA=\(\dfrac{mA}{nA}=\dfrac{16,25}{0,25}=65\) g/mol
\(\Rightarrow\) Kim loại A là kẽm (Zn)
b, Ta có pthh 2
Zn + H2SO4 \(\rightarrow\) ZnSO4 + H2
Theo đề bài ta có
nH2=\(\dfrac{5,04}{22,4}=0,225mol\)
Theo pthh
nZn=\(\dfrac{0,25}{1}mol< nH2=\dfrac{0,225}{1}mol\)
\(\Rightarrow\) Số mol của Zn thiếu
Theo pthh
nZn=nH2=0,225 mol
\(\Rightarrow\) Hiệu suất phản ứng là
Hs = (số mol phản ứng.100%)/số mol ban đầu = \(\dfrac{0,225.100\%}{0,25}=90\%\)
Cẩm Vân Nguyễn Thị em làm đúng ko cô