Viết phương trình điện li của các chất sau :
a) Các axit yếu : H2S, H2CO3.
b) Bazơ mạnh : LiOH.
c) Các muối: K2CO3, NaCIO, NaHS.
d) Hiđroxit lưỡng tính : Sn(OH)2.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

HS- H+ + S2-
HCO3- H + + CO32-
HS- H+ + S2-
H2SnO2 2H+ + SnO22-.

Viết phương trình điện li của các chất sau đây trong dung dịch :
1. Axit mạnh H2SeO4 (nấc thứ nhất điện li mạnh)
\(H_2SeO_4\rightarrow H^++HSeO_4^-\)
\(HSeO_4^-\leftrightarrow H^++SeO_4^{2-}\)
2. Axit yếu 3 nấc H3PO4
\(H_3PO_4\leftrightarrow H^++H_2PO_4^-\)
\(H_2PO_4^-\leftrightarrow H^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
3. Hiđroxit lưỡng tính Pb(OH)2
\(Pb\left(OH\right)_2\leftrightarrow Pb^{2+}+2OH^-\)
\(Pb\left(OH\right)_2\leftrightarrow PbO_2^{2-}+2H^+\)
4. Na2HPO4
\(Na_2HPO_4\leftrightarrow2Na^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
5. NaH2PO4
\(NaH_2PO_4\leftrightarrow Na^++H_2PO_4^-\)
\(H_2PO_4^-\leftrightarrow H^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
6. Axit mạnh HMnO4
\(HMnO_4\rightarrow H^++MnO_4^-\)
7. Bazơ mạnh RbOH
\(RbOH\rightarrow Rb^++OH^-\)

Các axit yếu H2S; H2CO3:
H2S ⇆ H+ + HS-
HS- ⇆ H+ + S2-
H2CO3 ⇆ H+ + HCO3-
HCO3- ⇆ H+ + CO32-

Axit: là những chất phân li trong nước ra ion H+
Ví dụ:
HCl → H+ + Cl-
H2S ⇌ 2H+ + S2-
- Axit một nấc: là những axit chỉ phân li một nấc ra ion H+ thí dụ như HCl, HBr…
HCl → H+ + Cl-
- Axit nhiều nấc là những axit phân li nhiều lần ra H+
Ví dụ:
| H2S là axit hai nấc | H2S ⇔ H+ + HS- HS- ⇌ H+ + S2- |
| H3PO4 là axit ba nấc | H3PO4 ⇌ H+ + H2PO4- H2PO4- ⇌ H+ + HPO42- HPO42- ⇌ H+ + PO43- |

Các muối K2CO3, NaClO, NaHS
K2CO3 → 2K+ + CO32-
NaClO → Na+ + ClO-
NaHS → Na+ + HS-
HS- ⇆ H+ + S2-
a) H2S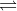 H+ + HS- ;
H+ + HS- ;
HS-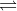 H+ + S2-
H+ + S2-
H2CO3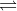 H+ + HCO3- ;
H+ + HCO3- ;
HCO3-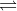 H + + CO32-
H + + CO32-
b) LiOH \(\rightarrow\)Li+ + OH-
c) K2CO3 \(\rightarrow\)2K+ + CO32- ;
NaClO \(\rightarrow\) Na+ + CIO-
NaHS \(\rightarrow\) Na+ + HS-:
HS-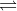 H+ + S2-
H+ + S2-
d) Sn(OH)2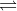 Sn2++ 2OH-;
Sn2++ 2OH-;
H2SnO2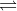 2H+ + SnO22-.
2H+ + SnO22-.