cho 2,4g Mg tác dụng với 9,8g H2SO4 , sau khi phản ứng xảy ra hoàn toàn thu đuocjw a gam muối và V lít khí H2 ở đktc. Hỏi sau phản ứng chất nào còn dư và dư bao nhiêu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Mg}=\dfrac{2.4}{24}=0.1\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.1....................................0.1\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(2H_2+O_2\underrightarrow{^{t^0}}2H_2O\)
\(0.1.....0.05\)
\(m_{O_2\left(dư\right)}=\left(0.5-0.05\right)\cdot32=14.4\left(g\right)\)

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

Nếu có thể thì lần sau bạn nên đăng tách từng bài ra nhé!
Bài 1:
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,1}{2}\) , ta được Mg dư.
Theo PT: \(n_{Mg\left(pư\right)}=n_{MgCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,05\left(mol\right)\)
\(\Rightarrow n_{Mg\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\)
\(\Rightarrow m_{Mg\left(dư\right)}=0,05.24=1,2\left(g\right)\)
\(m_{MgCl_2}=0,05.95=4,75\left(g\right)\)
\(V_{H_2}=0,05.22,4=1,12\left(l\right)\)
Bài 2:
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{14,7}{98}=0,15\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{2}>\dfrac{0,15}{3}\) , ta được Al dư.
Theo PT: \(\left\{{}\begin{matrix}n_{Al\left(pư\right)}=\dfrac{2}{3}n_{H_2SO_4}=0,1\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{H_2SO_4}=0,05\left(mol\right)\\n_{H_2}=n_{H_2SO_4}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{Al\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
\(\Rightarrow m_{Al\left(dư\right)}=0,1.27=2,7\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
Bài 3:
PT: \(2M+6HCl\rightarrow2MCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{4,704}{22,4}=0,21\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{3}n_{H_2}=0,14\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{3,78}{0,14}=27\left(g/mol\right)\)
Vậy: M là nhôm (Al).
Bài 4:
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=0,2\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Ta có: \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{4}>\dfrac{0,2}{5}\) , ta được P dư.
Theo PT: \(n_{P_2O_5}=\dfrac{2}{5}n_{O_2}=0,08\left(mol\right)\)
\(\Rightarrow m_{P_2O_5}=0,08.142=11,36\left(g\right)\)
Bạn tham khảo nhé!

\(n_{Mg}=0,08\left(mol\right)\)
\(n_{N_2O}=0,01\left(mol\right)\)
Bảo toàn e:
\(2n_{Mg}=8n_{NH_4^+}+8n_{N_2O}\)
\(\Rightarrow n_{NH_4^+}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg\left(NO_3\right)_2}=0,08\left(mol\right)\\n_{NH_4NO_3}=0,01\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{\text{muối}}=0,08.148+0,01.80=12,64\left(g\right)\)
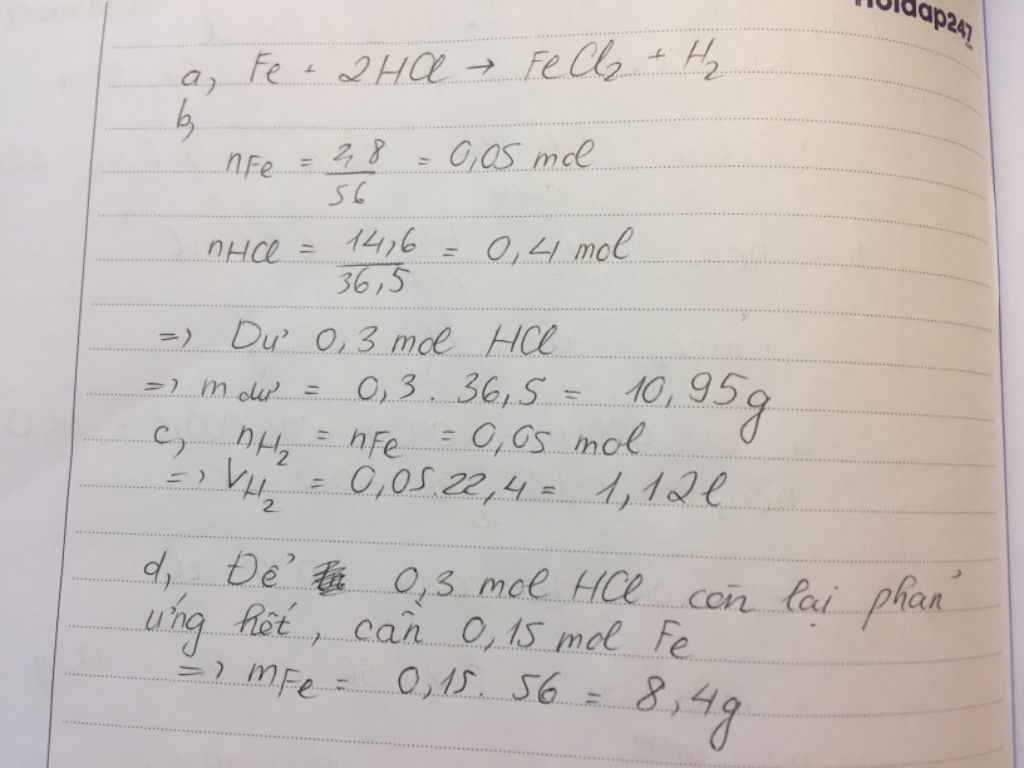



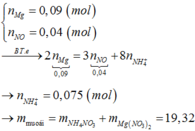
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
Theo PTHH, ta có: \(\dfrac{0,1}{1}=\dfrac{0,1}{1}\)
Kết luận: Không có chất dư
\(n_{MgSO_4}=n_{H_2}=n_{Mg}=0,1\left(mol\right)\)
\(m_{MgSO_4}=a=0,1.120=12\left(g\right)\)
\(V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)
Ta có: \(n_{Mg}=\frac{2,4}{24}=0,1\left(mol\right)\\ n_{H_2SO_4}=\frac{9,8}{98}=0,1\left(mol\right)\)
PTHH: Mg + H2SO4 -to-> MgSO4 + H2
Theo PTHH và đề bài, ta có:
\(\frac{0,1}{1}=\frac{0,1}{1}\)
=> phản ứng trên hết nên tính theo \(n_{Mg}hayn_{H_2SO_4}\) đều được.