cho 31,84g hỗn hợp NaX và NaY (X,Y là 2 halogen ở 2 chu kỳ liên tiếp) vào dd AgNO3 dư thu được 57,34g kết tủa .Công thức của 2 muối là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)

TH1: NaF và NaCl
Kết tủa chỉ có AgCl
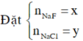
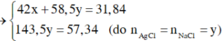
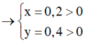
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
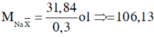
=> 2 muối là NaBr và NaI
Đáp án A

Cái chỗ M đó suy ra là \(M_X< 83,13< M_Y\)
Thì có 2 chất liên tiếp là Br (80) và I (127)

Nếu AgX và AgY đều kết tủa thì ta có:
NaX + AgNO3 -> AgX ↓ + NaNO3 (1)
a...........................a (mol)
NaY + AgNO3 -> AgY ↓ + NaNO3 (2)
Ta có hệ pt: \(\left\{{}\begin{matrix}\left(23+X\right)a+\left(23+Y\right)b=31,84\left(I\right)\\\left(108+X\right)a+\left(108+Y\right)=57,34\left(II\right)\end{matrix}\right.\)
Giải hệ pt ta đc: a + b = 0,3 (III)
Từ (I) => aX + bY = 24,94 (IV)
Gọi \(\overline{X}\) là khối lượng nguyên tử trung bình của X, Y, ta có:
\(\overline{X}\)=\(\dfrac{m_{hh}}{n_{hh}}=\dfrac{24,94}{0,3}=83,13\)
Vì X < \(\overline{X}\) < Y => X < 83,13 < Y
X = 80 < 83,13 nên X là brom và Y = 127 > 83,13 nên Y là iot
Vậy công thức của hai muối là NaBr và NaI
Đặt công thức hóa học 2 muối là NaZ.
Trong đó X<Z<Y
PHƯƠNG TRÌNH LÀ:
NaZ+AgNO3===>NaNO3+AgZ
Theo bài:
31,84/( 23+Z)=57,34/(108+Z)
Giải pt ta được Z=83,3333
Vì X,Y 2 chu kì liên tiếp=> X=Br Y=I.

(Bài này giải như bình thường thôi. Nhưng lưu ý với bạn là nếu có 1 muối là NaF thì muối này ko tạo kết tủa với AgNO3 đâu)
* Trường hợp 1: Ko có muối NaF
Gọi công thức tổng quát chung hai muối là: NaX.
Phương trình hoá học viết được:
NaX + AgNO3 = AgX + NaNO3
(23+X) (108+X) (g)
31,84 57,34
=> X=83,13 => Hai halogen là: Bx và I.
* Trường hợp 2: ! trong hai muối là NaF (giả sử là NaX)
Lúc đó chỉ có NaY phản ứng (chỉ có 3 khả năng: Cl, Br hoặc I thôi nên thử từng khả năng cũng được) => đáp án: Cl
Vậy 2 muối là NaF và NaCl hoặc NaBr và NaI.

Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br

a)
Giả sử cả 2 chất đều cho kết tủa
\(NaM+AgNO_3\rightarrow AgM+NaNO_3\)
\(n_{NaM}=n_{AgM}\)
\(\Leftrightarrow\frac{26,45}{23+M}=\frac{51,95}{108+M}\)
\(\Rightarrow M=65,167\left(\frac{g}{mol}\right)\)
\(\Rightarrow\left\{{}\begin{matrix}NaX:NaCl\\NaY:NaBr\end{matrix}\right.\)
b, Gọi số mol của NaCl là a, số mol của NaBr là b
\(\left\{{}\begin{matrix}58,5a+103b=26,45\\143,5a+188b=51,95\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)


là mày giết nhà mày đi