cho 1,41g hỗn hợp 2 kim loại Al và Mg tác dụng với dung dịch H2SO4 dư phản ứng xong thu được 1568ml khí đktc .Tính thành phần phần trăm theo khối lượng và theo số mol của mỗi kim loại trong hỗn hợp đầu
các bạn giúp mình vs ak mình cần gấp lắm . mình cảm ơn

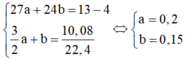
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2 (1)
2 3 1 3 ( mol)
2x 3x x 3x
Mg + H2SO4 -> MgSO4 +H2 (2)
1 1 1 1
y y y y
Gọi số mol của Al là x
=> nAl = 2x, nH2SO4 = 3x, nAl2(SO4)3= x , nH2= 3x
Gọi số mol của Mg là y
=> nMg = y, nH2SO4 = y, nMgSO4 = y, nH2= y
Ta có:
mhh = mAl + mMg
1,41= 27.2x + 24y
1,41= 54x + 24y
V H2 (1) + V H2 (2) = 1,568 (1568ml = 1,568 l)
22,4 . 3x + 22,4y = 1,568
67,2x + 22.4y = 1,568
Có : - 54x + 24y=1,41
- 67,2x + 22.4y = 1,568
Bấm máy tính => x = 0,015
y = 0,025
mAl = 54x = 54 . 0,015 = 0,81 9(g)
mMg = 1,41 - 0,81 = 0,6 (g)
%mAl = 0,81 . 100 / 1,41 = 57,45%
%mMg = 100% - 57,45% = 42,55%