BT 1 : Xác định thành phần % về khối lượng cua r các nguyên tố trong hợp chất : FeO : CO2 : CaCO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt : CTHH có dạng là : \(Na_xC_yO_z\)
\(\%Na=\dfrac{23x}{106}\cdot100\%=43.4\%\)
\(\Rightarrow x=2\)
\(\%C=\dfrac{12x}{106}\cdot100\%=11.3\%\)
\(\Rightarrow y=1\)
\(z=\dfrac{106-23\cdot2-12}{16}=3\)
CTHH có dạng là : Na2CO3

Đ
ặ
t
:
Y
(
N
O
3
)
2
V
ì
:
%
m
Y
=
34
,
043
%
⇔
M
Y
M
Y
+
124
=
34
,
043
%
⇔
M
Y
=
64
(
g
m
o
l
)
⇒
Y
:
Đ
ồ
n
g
(
C
u
=
64
)
⇒
C
T
H
H
:
C
u
(
N
O
3
)
2
Thu gọn

a)
Do R thuộc nhóm VA
=> CTHH của R và H là: RH3
Có \(\dfrac{3}{M_R+3}.100\%=17,64\%=>M_R=14\left(g/mol\right)\)
=> R là N
b) Do CTHH của R và H là RH3
=> oxit cao nhất của R là R2O5
Có: \(\dfrac{16.5}{2.M_R+16.5}.100\%=74,07\%=>M_R=14\left(g/mol\right)\)
=> R là N

\(\%Ca=\dfrac{1.40}{100}.100\%=40\%\\\%C=\dfrac{1.12}{100}.100\%=12\%\\ \%O=100\%-\left(40\%+12\%\right)=48\% \)
MCaCO3 = 100 g/mol
%Ca = \(\dfrac{40}{100}.100\)= 40%
%C = \(\dfrac{12}{100}.100\)= 12%
%O3= \(\dfrac{48}{100}.100\)=48%

Bài 2:
\(Đặt.CTTQ.của.A:H_xS_yO_z\left(x,y,z:nguyên,dương\right)\\ Ta.có:\left\{{}\begin{matrix}x=\dfrac{98.2,04\%}{1}=2\\y=\dfrac{98.32,65\%}{32}=1\\z=\dfrac{98.\left(100\%-2,04\%-32,65\%\right)}{16}=4\end{matrix}\right.\\ \Rightarrow x=2;y=1;z=4\\ \Rightarrow CTHH:H_2SO_4\)
Bài 1: Sửa đề 59,2% Al thành 52,9% Al
\(Đặt.CTTQ:Al_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{52,9\%.102}{27}\approx2\\ \Rightarrow y\approx\dfrac{\left(100\%-52,9\%\right).102}{16}\approx3\\ \Rightarrow CTHH:Al_2O_3\)

Câu 1 :
Dẫn CO2 đi qua H2SO4 (đ), H2SO4 (đ) hút nước mạnh và không phản ứng với CO2 từ đó làm khô được CO2
Câu 2 :
\(M_{FeO}=56=16=72\left(g\text{/}mol\right)\)
\(\%Fe=\dfrac{56}{72}\cdot100\%=77.78\%\)
\(\%O=100\%-77.78\%=22.22\%\)
\(M_{Fe_2O_3}=56\cdot2+16\cdot3=160\left(g\text{/}mol\right)\)
\(\%Fe=\dfrac{56\cdot2}{160}\cdot100\%=70\%\)
\(\%O=100\%-70\%=30\%\)
\(M_{H_3PO_4}=1\cdot3+31+16\cdot4=98\left(g\text{/}mol\right)\)
\(\%H=\dfrac{1\cdot3}{98}\cdot100\%=3.06\%\)
\(\%P=\dfrac{31}{98}\cdot100\%=31.63\%\)
\(\%O=100\%-3.06\%-31.63\%=65.31\%\)
\(M_{Na_2SO_4}=2\cdot23+32+16\cdot4=142\left(g\text{/}mol\right)\)
\(\%Na=\dfrac{23\cdot2}{142}\cdot100\%=32.39\%\)
\(\%S=\dfrac{32}{142}\cdot100\%=22.54\%\)
\(\%O=100\%-32.39\%-22.54\%=45.07\%\)

Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
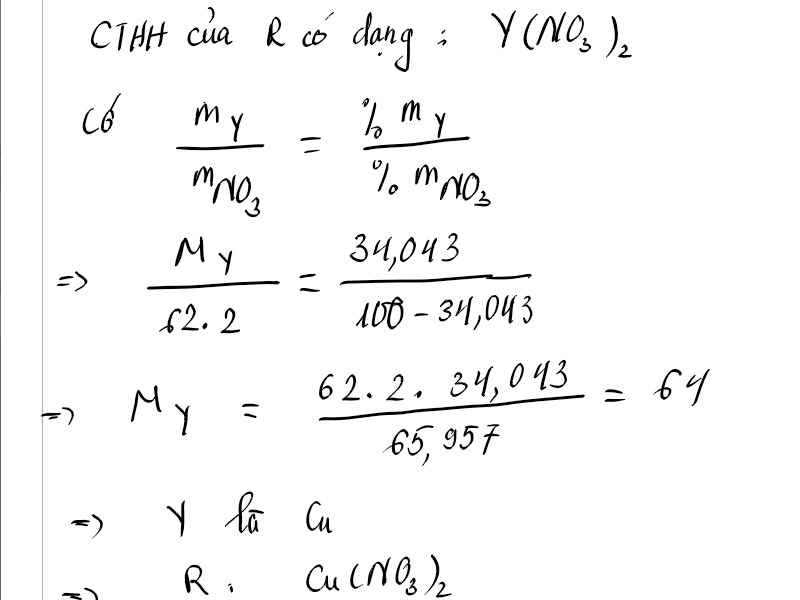
+ FeO
+ CO2
+ CaCO3
MFeO= 72 g/mol
%Fe = ( 56 .100):72 =77,7%
%O = (16.100):71 =22,3 %
MCO2=44g/mol
%C = (12.100): 44= 27,27%
%O = ( 32.100):44 = 72,73%
MCaCO3=100g/mol
%Ca = ( 40.100):100 = 40%
%C = (12.100):100 = 12%
%O = (48 . 100):100 = 48%